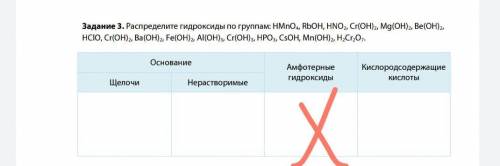
Задание 3. Распределите гидроксиды по группам: HMnO4, RbOH, HNO, Cr(OH)2, Mg(OH),, Be(OH), HaO, Cr(OH), Ba(OH)2, Fe(OH)2, Al(OH)3, Cr(OH)3, HPO3, CsOH, Mn(OH)2, H,Cr,07.
Основание
Амфотерные
гидроксиды
Кислородсодержащие
кислоты
Щелочи
Нерастворимые
Химические свойства оснований
В
Другие вопросы по теме Химия
Популярные вопросы
- Есть у меня дом большой, да только, вот, больно ветхим стал – крыша...
2 - Определить значение x соответствующее значению y=0 для линейного уравнения...
1 - Скласти 5 речень з майбутнім часом...
1 - Выполни частичный синтаксический разбор предложения по следующей схеме:...
2 - 1. Айдың тұтылуы дегеніміз не?А) Айдың Жер көлеңкесінде қалу құбылысыБ)...
2 - Сделайте 2 номер нужно. С меня ...
2 - C+H2O=CO+H2 подпишите названия веществ...
3 - Во и задания1. Что такое основной алгоритм, вс алгоритм?2. Чем отличается...
3 - Привет Нужна история создания вертела,и в чем особенность жарки на нем...
1 - Ели ab =0, то ... или ... а равно 0 а равно b b равно 0...
3
Шаг 1: Разберемся с группой "Основание". Основаниями называются вещества, которые в растворе образуют ион гидроксида (OH-) и способны принимать протоны (H+). В данном случае, группой "Основание" являются вещества, которые содержат ион гидроксида.
Гидроксиды из данного списка, относящиеся к группе "Основание":
1. RbOH (рубидиевый гидроксид)
2. Mg(OH)2 (магниевый гидроксид)
3. Be(OH)2 (бериллий гидроксид)
4. Ba(OH)2 (барий гидроксид)
5. Fe(OH)2 (железный(II) гидроксид)
6. Al(OH)3 (алюминиевый гидроксид)
7. Cr(OH)3 (хромовый(III) гидроксид)
8. Mn(OH)2 (марганцевый(II) гидроксид)
Шаг 2: Теперь рассмотрим группу "Амфотерные гидроксиды". Амфотерные гидроксиды могут действовать как кислоты, так и основания. В данном случае, следующие гидроксиды принадлежат к этой группе:
1. Cr(OH)2 (хромовый(II) гидроксид)
2. Cr(OH) (хромовой гидроксид)
Шаг 3: Теперь рассмотрим группу "Кислородсодержащие кислоты". Кислородсодержащие кислоты - это вещества, в которых присутствует один или более атомов кислорода. В данном списке такие гидроксиды:
1. HMnO4 (марганцевая кислота)
2. HNO (азотная кислота)
3. H,Cr,07 (хромухлористовая(IV) кислота)
4. HPO3 (фосфористая кислота)
Шаг 4: Рассмотрим группу "Щелочи". Щелочи - это гидроксиды щелочных металлов. В данном списке есть одно щелочное гидроксидное вещество:
1. CsOH (цезиевый гидроксид)
Шаг 5: Теперь рассмотрим группу "Нерастворимые". Нерастворимые гидроксиды - это гидроксиды, которые практически не растворяются в воде. В данном списке такие гидроксиды:
1. Cr(OH) (хромовый гидроксид)
Шаг 6: Наконец, рассмотрим группу "Химические свойства оснований". Данные свойства варьируются в зависимости от вещества, поэтому необходимо их подробно изучать в отдельности.
Вот и все! Мы разобрали все гидроксиды и распределили их по соответствующим группам. Если у вас возникнут еще вопросы, пожалуйста, не стесняйтесь задавать их.