При изминение температуры газа от 13градусов до 52 его давление повысилась на 117мм ртутного столба.найтти первоначальное давление газа,если его объем не изменился?
Другие вопросы по теме Физика
Популярные вопросы
- Разобрать слова по составу(корень суфикс и т.д.) подводный акваланг лошадки картошечка...
3 - Вставь в эти предложения how much, how many или a lot of....
3 - В. караленко ,,дети подземелья какие открытия сделал для себя вася, общаясь с...
3 - Каковы правила поведения за столом во время трапезы...
1 - Ch4 ch3-ch2-ch3 ( используя только неорганические реактивы)...
2 - Подобрать однокоренные слова к слову проблема...
2 - Осуществить превращения al - al2o3 - kalo2 - kcl - agcl....
3 - Вдвух одинаковых мотках было одинаковое количество провода. из первого мотка отмотали...
3 - Нормальная по составу крови женщина в браке с мужчиной гемофиликом у них родились...
2 - Под шатром широким кругом мчатся кони друг за другом, стройные, , сбруи . едут...
1
Запишем уравнение Менделеева-Клапейрона:
В первом состянии: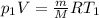
Во втором состоянии: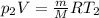
Так как давление увеличилось, то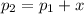 а
а 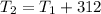 в Кельвинах
в Кельвинах
Делим второе на первое, чтобы узнать отношение давлений:
x=117мм. ртутного столба=117*133Па=15*10^5 Па
его объем не изменился V=const
T1 = 13 C+273 =286 K
T2 = 52 C+273 =325 K
dT=117 мм.рт.ст.
p1V = vRT1 - состояние (1)
p2V= vRT2 - состояние (2)
разделим (1) на (2)
p1V /p2V = vRT1/vRT2
p1 /p2 = T1/T2
p1*T2 = p2*T1 p2=p1+dp
p1*T2 = (p1+dp)*T1
p1*T2 = p1T1+dp*T1
p1*T2 - p1T1=dp*T1
p1=dp*T1 / (T2-T1) = 117*286 / (325-286) = 858 мм.рт.ст.
ответ 858 мм.рт.ст.