Вычислите массу соли образующейся при взаимодействии 49 г серной кислоты с оксидом меди 2
Другие вопросы по теме Химия
Популярные вопросы
- Почему небо синее? и обложка когда задаешь во...
1 - Денис загадал четыре различных натуральных числа. Он утверждает,...
1 - Де поширений чорнозем в Україні а) полісся; б) південний берег Криму;...
2 - А)10м 6 см- 8 дм 7 см= б) 250 мин 48 сек+ 50 мин 32 сек= в) 6 т...
2 - 1)Расставьте знаки препинания и буквы. 2) Подчеркните уточняющие...
1 - 1)У якому стані речовина передає створений нею тиск тільки в напрямку...
1 - 5. Океаническая земная кора имеет строение:а) трехслойноев) двухслойноеб)...
1 - со 1.2 задание нужно если с делаете. за раней говорю...
3 - Символом єднання у боротьбі з ВІЛ-СНІДом з 1991 року є червона стрічка....
3 - 12. Расскажите о дружбе Грэя и Бетси. Какой благородный поступок...
1
ответ: m(CuSO₄) = 80г
Объяснение:
H₂SO₄ + CuO = CuSO₄ + H₂O
m(H₂SO₄) = 49г
M(H₂SO₄) = 2 + 32 + 16 × 4 = 98 г\моль
n(H₂SO₄) =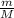 =
= 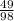 = 0.5 моль
= 0.5 моль
n(H₂SO₄) = n(CuSO₄) = 0.5 моль (по уравнению реакции)
M(CuSO₄) = 64 + 32 + 16 × 4 = 160 г\моль
m(CuSO₄) = n × M = 0.5 моль × 160 г\моль = 80г