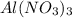Вычислить количество вещества, соответствующее: 490г h2so4; 9.8г h3po4 записать формулы солей: карбонат калия, сульфид свинца(ii), нитрат железа(iii); хлорид свинца (iv), фосфат магния, нитрат алюминия. из следующих формул выписать
оксиды, кислоты, основания, соли. дать названия
Другие вопросы по теме Химия
Популярные вопросы
- Прочитайте отрывок из произведения Пришвина Кладовая солнца и...
1 - Реши уравнение: |y|=22. Выбери правильный вариант (варианты) ответа:...
3 - Спиши предложение, расставив знаки препинания, вставляя пропущенные...
3 - Tasks for the Summative Assessment for the term 4Grade 6Task I....
2 - ХЕЛП! Электростатика задачи...
3 - Які пороки людства розкриті в представниках планет, що відвідав...
2 - Как выжить в пустыне от первого лица...
1 - 2. Данные глаголы запишите в таблицу, образуя указанные формы....
2 - Прочитать рассказ Остров М. М. Пришвина. Кратко написать, о чём...
3 - Точки А(-3;-2), В(-1; 2), C(5;2) и D являются вершинами параллелограмма...
3
1. n = m/M
M(H2SO4) = 1*2 + 32 + 16*4 = 98 г/моль
n(H2SO4) = 490 г / 98 г/моль = 5 моль
M(H3PO4) = 1*3 + 31 + 16*4 = 98 г/моль
n(H3PO4) = 9,8 г /98 г/моль = 0,1 моль
2. Карбонат калия -K2CO3
сульфид свинца (II)- PbS
нитрат железа (III) -Fe(NO3)3
хлорид свинца (IV) -PbCl4
фосфат магния -Mg3(PO4)
нитрат алюминия - Al(NO3)3
3. H2S, K2So3, KOH, SO3,Fe(OH)3, FeO, N2O3, Cu3(PO4)2, Cu2O, P2O5, H3PO4
Оксиды: SO3, FeO, N2O3, Cu2O, P2O5.
Кислоты: H2S, H3PO4.
Основания: КОН, Fe(OH)3.
Соли: K2So3, Cu3(PO4)2.
Карбонат калия-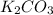
сульфид свинца(II)-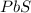
нитрат железа(III)-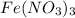
хлорид свинца (IV)-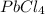
фосфат магния-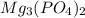
нитрат алюминия-