Визначте молекулярну формулу вуглеводню, якщо під час спалювання його кількістю речовини 0,1 моль утворюється вода масою 5,4 і вуглекислий газ об'ємом 8,96 л (н.у.)
Другие вопросы по теме Химия
Популярные вопросы
- Скажите как будет правильно на предложение: она немного ниже меня...
3 - Решить в столбик 30075: 401, 73278: 354...
1 - Найди половину произвеления 5*(74*4)...
3 - Решите уравнение 5(2x - 7) = 3(3x + 7)...
2 - 4)найдите архимедову силу, действующую в воде на брусок размером 2х5х10...
1 - Поставьте глаголы в предложениях в отрицательную и вопросительную...
2 - Повідомлкння про батьківщину туве янсон...
2 - Однажды вечером кончив дневной сбор винограда молдаване ушли на берег...
2 - Где днепр берет начало и куда впадпет...
2 - Создерди соз таптарына топтап жаз, кунделик, курт,молдир ,мын,алтыншы,...
2
Задача: Определите молекулярную формулу углеводорода, если при сжигании его количеством вещества 0,1 моль образуется вода массой 5,4 г и углекислый газ объемом 8,96 л (н.у.).
Дано:
n (CxHy) = 0,1 моль ;
m (H₂O) = 5,4 г ;
V (CO₂) = 8,96 л.
Найти:
x, y (формулу) — ?
1. Вычислим количество вещества воды и углекислого газа по формулам: n = m : M и n = V : Vm; где: n - количество вещества (моль), m - масса (г), M - молярная масса из таблицы (г/моль), V - объём (л), Vm - молярный объём газов, постоянная величина, равная 22,4 (л/моль) при н.у.
n (H₂O) = 5,4 г : 18 г/моль = 0,3 (моль).
n (CO₂) = 8,96 л : 22,4 л/моль = 0,4 (моль).
2. Используя правило, найдём массы углерода и водорода в углеводороде.
n (C) = n (CO₂) ; n (H) = 2n (H₂O), соответственно ⇒
n (C) = 0,4 (моль); n (H) = 0,3 · 2 = 0,6 (моль).
Из вышеописанной формулы (n = m : M) выразим массу и найдём её для каждого элемента в соединении.
m (C) = 0,4 моль · 12 г/моль = 4,8 (г).
m (H) = 0,6 моль · 1 г/моль = 0,6 (г).
Тогда, m (CxHy) = 4,8 + 0,6 = 5,4 (г).
3. Мы нашли массу углеводорода, а также нам в условии дано его количество вещества. По вышеописанной формуле (n = m : M) выразим молярную массу и найдём её.
M (CxHy) = 5,4 г : 0,1 моль = 54 (г/моль).
4. Но нам это ничего не даёт, поэтому нам нужно найти мольное соотношение углерода и водорода.
C : H =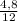 :
: 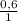 = 0,4 : 0,6 = 4 : 6 = 2 : 3.
= 0,4 : 0,6 = 4 : 6 = 2 : 3.
Итак, простейшая формула: C₂H₃. Но её молярная масса = 27 г/моль, а нам нужно 54 г/моль.
Из этого следует, что истинная формула: C₄H₆.
ответ: C₄H₆.