Определите массу хлора для хлорирования смеси меди и железа массой 60 г. Массовая доля меди в смеси = 53.3%. В результате реакции образуется хлорид меди 2 и хлорид железа 3. Мои расчёты :
m (Cu) = 31.98 г
m (Fe) = 28.02 г
Потом я вычислила кол-во в-ва железа и меди
n(Cu) = 0.5 моль
n(Fe)=0.5 моль
Дальше я не понимаю как решать
Другие вопросы по теме Химия
Популярные вопросы
- с геометрией. Через вершину конуса под углом α к плоскости его основания проведена...
3 - Самостійна робота з графіками. Залежність фотосинтезу від чинників довкілля....
1 - , очень ! 1. У бутана и гексана: А) Есть гомологи Б) Нет гибридизации В) Есть...
3 - Укажіть функцію, яка зростає на проміжку хє 2 A А Б В T д y=2 sin x y = cosx...
1 - 2. Известно, что 3 т 7 и 2 а) т + п б) т — п в) т • п г) т : п...
2 - Вынесите общий множитель за скобки2ах+6аb=...
2 - 7. Соотнесите: 1)Сунь Ятсен A) наследник китайского престола 2) Юань Шикай...
1 - Знайдти градусну міру кута SNP...
1 - Решите все на этой странице...
3 - Укажите функции, график которых проходят через точку (0;0): А) y=3x Б) y=sin...
2
88,75 г
Объяснение:
Продолжение расчетов.
Записываем уравнение: Cu+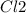 =CuCl2
=CuCl2
Видно, что использовали и там и там одинаковое количество, то есть 0,5 моль
Теперь найдем количество хлора, необходимого для реакции с железом
2Fe+3Cl2=2FeCl3
Из уравнения реакции видно , что
Находим общее количество требуемого хлора 0,5 моль+0,75 моль = 1,25 моль
Далее, вычисляем массу:
m(Cl2)=V(Cl2)*M(Cl2) = 1.25 моль*71 г/моль=88,75 г