Определите формулу газообразного соединения бора с водородом, если массовая доля бора в нем составляет 78,2 %, а масса одного литра этого газа равна массе 1 л азота.
Другие вопросы по теме Химия
Популярные вопросы
- Янашел ас и вd вместе. а как найти их по отдельноости....
3 - Написать коротко о чём гарри поттер 5-10 предложений...
3 - Сообщение на тему значения плесневых грибов. заранее...
2 - Записать краткую запись к этой решения не нада. семейный бюджет составляет...
1 - Нужна какая-то информация по теме «изомеры в природе» лучше чтобы информация...
1 - Сделать схемы следующих элементов: be,o,mg,s,ca...
3 - Примеры длительности из жизни своей...
3 - Образуйте по 1 существительное и 1 прилагательное слова приставочно суффиксальным...
3 - Начертите ленту времени. отметьте на ней события, указанные в . что произошло...
3 - Что происходит с пассажирами автобуса при его резком торможении? разгоне?...
2
1. Определим массу 1 моль соединения бора:
1 моль азота, а это 22,4 л имеет вес 28 г, а значит и соединение бора имеет вес 28 г
2. Теперь определим количество атомов бора и водорода:
Вот и выходит формула: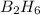
Молярная масса соед-ия сос-т 28 г/моль (раз 1 л соед-ия имеет массу равную массе 1 л азота, след-но 22.4 л соед-ия имеет массу = массе 22.4 л азота (M N2 = 28 г/моль)); т.о. кол-во в-ва B сос-т (28*0.782)/11 = 2 моль, а кол-во в-ва H - соот-но (28*(1-0.782))/1 = 6 моль, что приводит к прос-й ф-ле B2H6 (M = 28 г/моль, след-но простейшая ф-ла явл-ся истинной ф-ой).