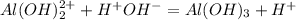Определить среду водных растворов солей: na3po4, ca(no3)2, k2co3, alcl3. составте уравнения реакции гидролиза.
Другие вопросы по теме Химия
Популярные вопросы
- Продам мёд Куда писать вопросу почту напишу в кометах...
2 - вычислите площадь фигуры, ограниченной фигуры...
2 - Etер - BilimLand х+x2.2020/lesson/88a08cb8-fa7d-4e10-8094-3628792a23ec::Прочитай...
2 - Write a letter to a friend about your last holiday...
3 - Напишите текст на одну из предложенных тем. Соблюдайте логичность и последовательность...
3 - упростите выражение (2a-9) -2(5a+4) -3 найдите его значение при решите у меня СОЧ...
1 - Основания равносторонней 5м и 11м, а боковая стенка 5м. Найдите высоту трапеции?...
2 - Решите неравенство 3tg2x корень из 3...
2 - RiRGOSORHR.R.? tampogutin...
2 - у= 2/х - гипербола и у=2х^2 парабола....
2
1 соль
1 ступень:
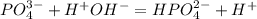
2 ступень:

3 ступень:
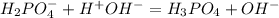
2 соль
3 соль
1 ступень:
2 ступень:
4 соль
1 ступень:
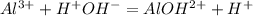
2 ступень:
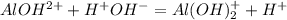
3 ступень: