НУЖНО РЕШЕНИЕ , ОТВЕТ ЕСТЬ Определить константу диссоциации NH4ОН, если эквивалентная
электрическая проводимость 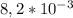 М раствора его равна 12,43 См*см^2/моль экв.
М раствора его равна 12,43 См*см^2/моль экв.
ответ: 1,67*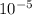
Распишите решение, ответ есть
Другие вопросы по теме Химия
Популярные вопросы
- У циліндрі паралельно його осі проведено площину, яка перетинає основу циліндра...
1 - Запишите все названия четырёхугольников надо хотя бы 10...
3 - Материальная точка движется под действием системы сил F1=10H F2=20H F3=15H, m=10кг....
2 - Сколько бит составляет сообщение, содержащее 0,8 Кб?...
2 - Наименьшее общее делимое 59049и729 32768и512...
2 - 1. Возьмите любой текст по вашей специальности.(2-3 )абзаца. 2. Прочитайте внимательно...
3 - Найди произведение 9/26×13/45 кому не трудно...
3 - Доклад на тему Я выбераю профессию...
1 - X²-x-72=0 имеет два корня1) 2)x²+x²...
1 - 1/4х+1/3х =8/15у - 2/5у=3/4т - 1/6т= помагите...
2
Λ = κ * С,
где Λ - эквивалентная электрическая проводимость, κ - константа диссоциации и С - концентрация раствора в молях.
В данном случае, нам дано значение эквивалентной электрической проводимости (Λ = 12,43 См*см^2/моль экв.) и нужно найти константу диссоциации.
Нам также дано, что концентрация раствора равна 8,2 × 10^(-3) М.
Мы можем подставить эти значения в уравнение и найти константу диссоциации:
12,43 См*см^2/моль экв. = κ * 8,2 × 10^(-3) М.
Чтобы найти κ, необходимо разделить обе стороны уравнения на 8,2 × 10^(-3) М:
κ = (12,43 См*см^2/моль экв.) / (8,2 × 10^(-3) М).
Осуществим вычисления:
κ = 12,43 / 8,2 × 10^(-3) = 1514,63 моль * См^(-1).
Теперь нам нужно выразить эту константу в нужной форме. Мы должны сократить моль См^(-1) до моль^(-1). Для этого нам нужно умножить числитель и знаменатель на 100 См:
κ = (1514,63 моль * См) / (8,2 × 10^(-3) М * 100 См) = 1514,63 * 100 моль / Кг.
Теперь мы должны привести эту константу к требуемой форме, что состоит из моль * Кг. Для этого мы должны умножить числитель и знаменатель на 10^(-3) Кг:
κ = (1514,63 * 100 моль * 10^(-3) Кг) / (8,2 × 10^(-3) М * 100 См * 10^(-3) Кг) = 151,463 моль / Кг.
Таким образом, значение константы диссоциации NH4ОН равно 151,463 моль / Кг.