Найти молекулярную массу углеводорода,содержащий 81,8% углерода и 18,2%водорода.относительная плотность этого вещества по азоту равна 1,57
Другие вопросы по теме Химия
Популярные вопросы
- Точка а принадлежит отрезку cd. длина cd=8см 9мм, cа=3см 6мм. найти...
3 - Сколько было приказов в середине 17 века...
2 - Как происходит формирование характера?...
2 - На прямой отмечены точки a,b,c, так, что ab=27см, ac=11см, bc=16см....
1 - Основание ac равнобедренного треугольника abc равно 12. окружность...
2 - Решите бруска. первый покоится, второй движется по инерции без трения,...
3 - Маленькое выступление по изо на тему мир изобразительных искусств....
1 - Выражение ((a^2-36*b^2)/a^2)*(a/a+6*b) а потом подставьте а=квадратный...
3 - Составте формулу и дайте название трем изомерам, отвечающим формулу...
3 - Дано: угол с=30 градусам, ас=10см, вс=8см, через вершину а проведена...
3
1. Найдем относительную молекулярную массу углеводорода по относительной плотности: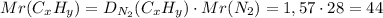
2.Теперь,с этой массы найдем количество атомов,сначала Углерода, а потом и Водорода: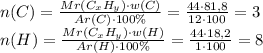
Значит формула углеводорода -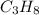 - это пропан
- это пропан