Найдите молекулярную формулу углеводорода, в составе которого масса углерода состовляет 0,827(82,7%), водорода 0,173(17,3%) , плотность по воздуху равна 2.
Другие вопросы по теме Химия
Популярные вопросы
- Правоведы при характеристике правомерного поведения отмечают,что большинство...
3 - Почему после подмораживания клубни картофеля становятся сладковатыми, плоды...
2 - 1.решите неравенство: x-5/2x-x^2 =0 2площадь прямоугольника равна 36 . какую...
2 - Запишите равенство и найдите y: число 162 больше,чем частное чисел 42 и y на...
1 - График линейной функции пересекают оси координат в точках 3: 0 и 0: -4 задать...
1 - Маша уронила 3 монеты. с какой вероятностью количество выпавших орлов будет...
2 - Y= 2 x ³ - 15 x ² + 36 x - 20 построить график функции с производной....
3 - Рассчитайте массу осадка полученного при взаимодействии раствора соли ,в котором...
2 - Что свидетельствовало о продолжении александром iii реформаторского курса? 1)...
2 - Печатная тетрадь по а.а.динилов и л.г.косулина страничка 76-77 6 класс надо:...
2
1. Сначала найдем молекулярную массу углеводорода через относительную плотность:
2. Теперь,если вспомнить формулу по определению массовой доли элемента в веществе и вывести из нее n - число атомов определенного элемента,то найдем и количество атомов Углерода и Водорода:
а)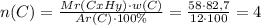
б)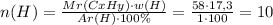
Значит формула углеводорода: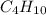 - это бутан
- это бутан