Народ вас. массовая доля, карбона в веществе составляет 51.89%, хлору- 38,38%, остальное - водород. относительная плотность випарив этого вещества по воздуху равна 3,19. установить истинную формулу вещества. под решением заранее вам!
Другие вопросы по теме Химия
Популярные вопросы
- У Ярослава были конфеты. Конфет с клубникой у него было в 2 раза...
2 - Правители государство эфталитов...
3 - 1. Расставить числа по возрастанию: 3F(16) ,124(8) ,10001(2) 2....
1 - Вынесите множитель из под знака корня: а)б)в)...
1 - нужно сделать «повідомлення на тему “використання топографічних...
3 - 3. Сравните объемы тел. Есть ли среди них равные?V. = 3,2 дм ;...
3 - На що вказують спільні ознаки між рослинною і твариною клітиною...
2 - с задачей (11кл) ЯП не важен...
2 - Да, да, мен, бен, пен шылау болса бөлек жазылады, жалғау болса...
3 - Аулада ойнап жүр едік, екі атты адам бір үйір түйені қуалай айдап,мал...
3
Объяснение:
1) Найдем процентное содержание водорода:
2) Найдем молярную массу вещества использую относительную плотность по воздуху:
Где M1 масса нужного нам вещества, а М2 масса вещества по которому высчитывается относительная плотность.
M2(масса воздуха)=29 г/моль
3) Найдем молярную массу каждого элемента в веществе:
Где M1 молярная масса элемента, а M2 молярная масса вещества, w массовая доля (Для перевода из % в доли надо поделить на 100%. Если массовая доля дана не в процентах то перевод не нужен).
4) Найдем число атомов элемента в веществе:
Где М1 молярная масса элемента в веществе, а М2 молярная масса одной атома элемента.
Получаем формулу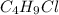
Для проверки найдем молярную массу вещества:
Молярная масса совпадает с найденной во 2-м пункте. Значит формула определенна верно.