M(h2so4)=98г
m(naoh) = 40г
какая соль - ?
m (соли) - ?
Другие вопросы по теме Химия
Популярные вопросы
- будбласка до ть ! ів написать 5 речень і над словом надписать частину мови...
2 - Культура Варнов Культура Кастов Культура Древнекитайской цевилизации Буду благодарна...
2 - 5-6 приложений о Генрихе Мореплавателе...
3 - 1.Определение значимости изучения географии Росии. 2.Создание ценностной шкалы...
3 - Какие важные исторические события были воспроизведены писателями в литературных...
2 - Докажите, что не имеет смысла выражение:...
3 - Алгебра. геометрическая прогрессия....
1 - Электрөткізгіштікті анықтайтын аспаптың шамы, оның электродтарын мыналардың...
3 - Из каких частей состоит песня Ах ты, степь широкая?...
3 - Відгук до билини про Іллю муромця та соловія ...
3
Проведем реакцию: H2SO4 + 2NaOH => Na2SO4 + 2H2O
ν (H2SO4) =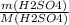 = 98 г : 98 г/моль = 1 моль
= 98 г : 98 г/моль = 1 моль
ν (NaOH) =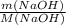 = 40 г : 40 г/моль = 1 моль
= 40 г : 40 г/моль = 1 моль
=> по расчетам ν (H2SO4) = ν (NaOH)
По уравнению реакции ν (H2SO4) : ν (NaOH) = 1:2 => NaOH взят в избытке, дальнейшие расчеты ведем по недостатку, то есть по H2SO4 =>
ν (H2SO4) = ν (Na2SO4) = 1:1
=> ν (Na2SO4) = ν (H2SO4) = 1 моль
m (Na2SO4) = ν (Na2SO4) * M (Na2SO4) = 1 моль * 142 г/моль = 142 г.
ответ: m (Na2SO4) = 142 г
P.S. Если из твоего краткого описания, я всё правильно понял, что с этим нужно делать, то вроде бы все правильно...