Ксерной кислоте прилили раствор , содержащий 10.4 хлорида бария. определите массу осадка
Другие вопросы по теме Химия
Популярные вопросы
- Запиши десятичную дробь в виде смешанного числа. в результате дробь сократи....
2 - Докажите, что 7 в шестнадцатой степени + 7 в четырнадцатой степени делится...
2 - Построить ув4-б6, ум7-ч5 в в g-moll(гарм) !...
1 - Мини-сочинение почему без растений жизнь на нашей планете будет невозможна?...
2 - Скласти план до твору»кумедія з костем»...
1 - Нужна .твiр на тему: яким має бути ставлення до грошей у людини?...
1 - Это по : ) молярная масса 1. сколько молекул содержится в 50,8 г йода?...
1 - Докажите что значение выражения принимает положительные значение при...
2 - Впредложении он пошёл было, но опять развернулся какой частью речи является...
2 - По , напишите 20 десятичных дробей ! буду !...
1
H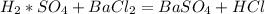
n=m/M
n(BaCl_{2})=10.4/207=0.05
n(BaCl_{2})=n(BaSO_{4})=0.05
m=n*M
m(BaSO_{4})=0.05*233=11.65
H2SO4 + BaCl2->BaSO4 + 2HCl
10.4г (BaCl2) - Xг(BaSO4)
208г/м - 233г/м
X=11,65г
если 10,4 л BaCl2, то вместо 208 подставь 22,4л/м