Какую массу эфира можно получить из 120 г уксусной кислоты и 120 г этанола, если массовая доля выхода продукта реакции составляет 80%?
Другие вопросы по теме Химия
Популярные вопросы
- 1. решите уравнение 5(x+4)=-9. 2. решите уравнение 3(x-8)+5x. 3. решите...
3 - Врезультате реакции сероводорода с кислородом при недостатке сумма коэффициентов...
1 - Модераторы не удаляйте . вообщем,мне 13 лет.я обленилась,нужно к экзамену...
3 - Докажите премьерами из текста что, жанр произведения л. толстого кавказский...
1 - Когда алиса помчалась в догонку за белым кроликом,то она провалилась в глубокий...
2 - Цитатная характеристика е.пугачева в поэме с.есенина пугачев...
3 - Keto rapid max in the affair digress you appeal to use it on customary start...
3 - Найти шестизначное число , произведения которого на n ( n=2,3,4,5,6) в произвольном...
2 - Кцентру тела вдоль одной прямой приложены три силы 5 н, 15 н и 20 н. чему...
3 - 1. определите силу тяжести, действующую: а) на человека массой m = 94 кг;...
2
CH₃COOH + C₂H₅OH = CH₃COOC₂H₅ + H₂O
1) Найдем количества каждого из реагирующих веществ, чтоб узнать, какое вещество дано в избытке:
M(CH₃COOH)=60 г/моль
M(C₂H₅OH)=46 г/моль
(уже, кстати, из молярных масс очевидно, что спирт дан в избытке, но мы все равно это проверим)
n(CH₃COOH)=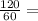 2 моль
2 моль
n(C₂H₅OH)=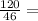 2,6 моль
2,6 моль
2) Расчет проводим по уксусной кислоте
M(CH₃COOH)=60 г/моль
M(CH₃COOC₂H₅)= 88 г/моль
m(CH₃COOH)= 120 г
m(CH₃COOC₂H₅)= х г
Расчет по уравнению реакции:
60 г CH₃COOH дают 88 г CH₃COOC₂H₅
120 г CH₃COOH дают х г CH₃COOC₂H₅
3) Найдем реальных выход эфира через пропорцию:
176 г - это 100% выхода
у г - это 80% выхода
ответ: можно получить 140,8 г эфира.