Дана схема превращений:
FeCl3 -->X-->Fe2(SO4)3 -->Fe(NO3)3
Напишите молекулярные уравнения реакций с которых можно осуществить указанные превращения. Для третьего превращения составьте сокращенное ионное уравнение реакции.
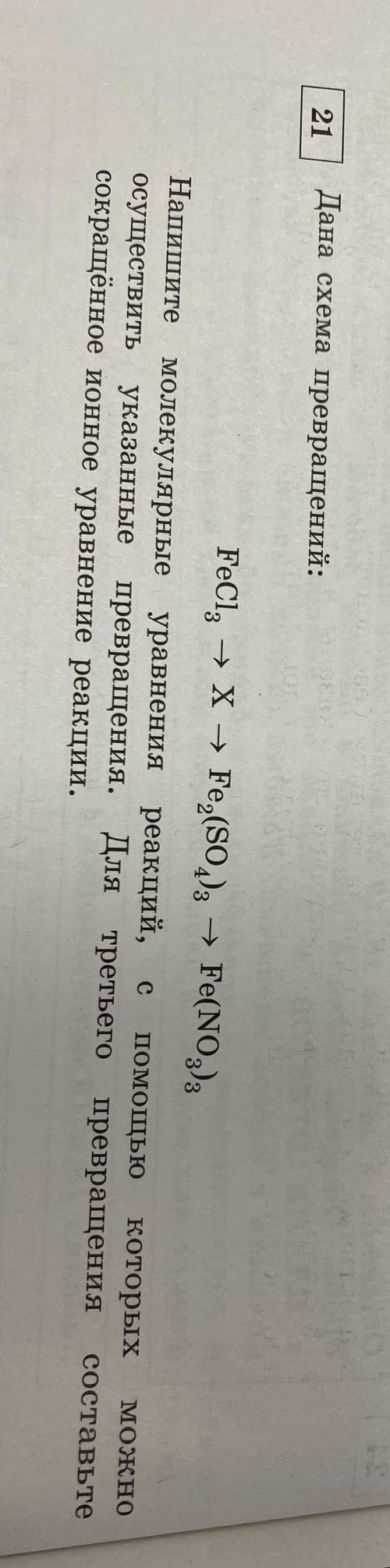
Другие вопросы по теме Химия
Популярные вопросы
- Укажите событие,к предпосылкам которого можно отнести введение сыска беглых...
3 - Разбейте число 10 на два неотрицательных слагаемых так чтобы сумма квадратов...
3 - Как решить это уравнение. 504/x=28*6...
1 - Эссе мы не можем ждать милостей от природы; взять их у нее - наша мы не можем...
3 - Какие народы населяют японию? каковы их основные занятия.?...
3 - Случаев,за которые мы можем попасть в суд,прокуратуру,полицию,фсб.(по одному...
1 - Сколько трехзначных чисел можно составить из цифр 0,2,4,6,8...
1 - Как определить размер малекулы масла? это по...
2 - На что направлены меры по охране природы?...
3 - Что такое дискуссия? 1) подготовьтесь к дискуссии на тему современная школа-достижения...
1
Объяснение:
FeCl3 + 3KOH = 3KCl + Fe(OH)3
2Fe(OH)3 + 3H2SO4 = Fe2(SO4)3 + 3H2O
Fe2(SO4)3 + 3Ba(NO3)2 = 2Fe(NO3)3 + 3BaSO4
Ba(2+) + SO4(2-) = BaSO4
Для начала, давайте рассмотрим первое превращение: FeCl3 --> ? --> Fe2(SO4)3.
Так как хлорид железа(III) содержит железо и хлор, а сульфат железа(III) содержит железо и сульфат, то можно предположить, что первая реакция будет происходить с сульфатом. Нужно найти соответствующий сульфат, который может превратить FeCl3 в Fe2(SO4)3.
Сульфат железа(II) (FeSO4) имеет такую же основную составляющую, что и сульфат железа(III) (Fe2(SO4)3), только в меньшей степени окисления. Так как окисление происходит с увеличением степени окисления, можно предположить, что можно использовать сульфат железа(II) для превращения FeCl3 в Fe2(SO4)3.
Mолекулярное уравнение первой реакции будет:
FeCl3 + FeSO4 -> Fe2(SO4)3 + FeCl2
Теперь рассмотрим второе превращение: Fe2(SO4)3 --> ? --> Fe(NO3)3.
Так как сульфат железа(III) содержит железо и сульфат, а нитрат железа(III) (Fe(NO3)3) содержит железо и нитрат, можно предположить, что реакция будет происходить с нитратом.
Нитрат железа(III) можно получить путем реакции Fe2(SO4)3 со свободной нитратной кислотой (HNO3):
Fe2(SO4)3 + 6HNO3 -> 2Fe(NO3)3 + 3H2SO4
Теперь мы можем представить сокращенное ионное уравнение для третьего превращения:
Fe2(SO4)3 + 6NO3- + 2H+ -> 2Fe3+ + 6NO3- + 3SO4^2- + 2H2O