1. Выберите два высказывания, в которых говорится об алюминии как о простом веществе.
1) Избыток алюминия в почве задерживает рост растений.
2) Алюминий растворяется в щелочах.
3) Массовая доля алюминия в его высшем оксиде составляет 53%
4) Электропроводность алюминия меньше электропроводности меди.
5) В природе алюминий достаточно распространен.
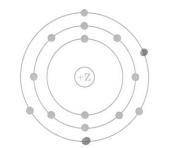
2. На приведенном рисунке изображена модель атома химического элемента
Запишите номер периода и номер группы, в которых расположен этот элемент.
3. Какие два утверждения верны для характеристики как магния, так и кальция?
1) На внешнем электронном слое находится 2 электрона.
2) Химический элемент образует просто вещество-неметалл.
3) Значение радиуса атома меньше, чем у рубидия.
4) Соответствующее простое вещество существует в виде двухатомных молекул.
5) Химический элемент образует высший оксид с общей формулой ЭО2.
4.Какие два из перечисленных веществ вступают в реакцию с оксидом бария?
1) Ва(OH)2 2) H2SO4 3) FeSO4 4) CO2 5) NaOH
5. Установите соответствие между исходным(и) веществом(-ами) и продуктами реакции: к
каждой позиции, обозначенной буквой, подберите соответствующую позицию,
обозначенную цифрой.
ИСХОДНЫЕ ВЕЩЕСТВА ПРОДУКТЫ РЕАКЦИИ
А) Fе+ HCI → 1) FeCI3 + Н2
Б) Fe2O3 + HCI → 2) FeCI2+ H2O
В) Fe3O4→ 3) FeCI3+ H2O
4) FeCI2 + Н2
5) FeCI2 + FeCI3 + Н2O
6. Установите соответствие между названием вещества и реагентами, с которыми это
вещество может взаимодействовать.
НАЗВАНИЕ ВЕЩЕСТВА РЕАГЕНТЫ
А) кальций 1)HBr, N2
Б) хлорид бария 2)Na2SO4, K3PO4
В) гидроксид натрия 3)H2О, KOH
4) H2SO4, AI(ОН)3
7. Из предложенного перечня выберите две пары веществ, между которыми протекает
реакция обмена.
1) алюминий и соляная кислота
2)оксид бария и гидроксид натрия
3) натрий и кислород
4)гидроксид алюминия и серная кислота
5) хлорид калия и нитрат серебра
8. Вычислите в процентах массовую долю железа в нитрате железа(II)
9. Дана схема превращений: Ва(OH)2 → X → BaO → BaCI2
Напишите молекулярные уравнения реакций, с которых можно осуществить
указанные превращения. Для первого превращения составьте полные и краткие ионные
уравнения.
10. К раствору фосфата натрия массой 53 г и массовой долей 5% прилили избыток раствора
хлорида меди (II). Вычислите массу образовавшегося осадка.
Другие вопросы по теме Химия
Популярные вопросы
- срочоно задание, очень Доведіть, що ΔАВС — рівностороннійЗнайдіть ABC...
1 - Решите уравнение очень надо до 20:00 (у^3+4у^2-6)-(5у-у^3+6)=2у^3+4у^2+у...
3 - Немецкий язык, нужно сделать 8, 9, 10...
3 - Көбейткіштерге жіктеп, бос орындарды толтыр. c3k + d6k = (ck) + (d )3 = (ck...
3 - Activity 3. What would you have as a main meal, side dish, dessert and drink...
3 - Зар-заман ақындарына кімдер жатады?...
1 - Як вчинив ворожий солдат в повісті Климко коли знайшов у полі під скиртою...
1 - (Создайте словесный портрет Молчалина и Скалозуба.) (Заполните таблицу краткими...
3 - До ть! ів, прикріпила фото! Прочитати текст і вибрати з A-H підходяще і вставити...
1 - 2. ( ). Вибрати приклад правильного порівняння виразів: а) -58 55; б) 0.7...
1
Из предложенных высказываний, соответствующими определению простого вещества будут высказывания:
- 2) Алюминий растворяется в щелочах.
- 5) В природе алюминий достаточно распространен.
2. Для определения номера периода и номера группы элемента на рисунке, необходимо знать расположение элементов в таблице химических элементов.
На рисунке представлена модель атома, обозначена ядерная оболочка, электронные оболочки и электроны.
Номер периода определяется по количеству электронных оболочек (горизонтальное положение элемента в таблице химических элементов). Номер группы определяется по количеству электронов на внешней электронной оболочке (вертикальное положение элемента).
3. Для определения верных утверждений для характеристик магния и кальция, необходимо проверить каждое утверждение отдельно и сравнить с характеристиками магния и кальция.
Верными утверждениями для характеристик и магния, и кальция будут:
- 1) На внешнем электронном слое находится 2 электрона.
- 4) Соответствующее простое вещество существует в виде двухатомных молекул.
4. Для определения двух веществ, вступающих в реакцию с оксидом бария, необходимо знать, какие вещества могут взаимодействовать с оксидом бария.
Оксид бария имеет формулу BaO, поэтому вещества, вступающие в реакцию с оксидом бария, должны содержать соответствующие реагенты и способствовать образованию новых веществ.
Из предложенных веществ, вступающих в реакцию с оксидом бария будут:
- 1) Ва(OH)2
- 4) CO2
5. Для установления соответствия между исходными веществами и продуктами реакции, необходимо проверить каждое исходное вещество с каждым продуктом реакции.
- ИСХОДНЫЕ ВЕЩЕСТВА:
- A) Fе + HCI → 1) FeCI3 + Н2
- Б) Fe2O3 + HCI → 2) FeCI2 + H2O
- В) Fe3O4 → 3) FeCI3 + H2O
- 4) FeCI2 + Н2
- 5) FeCI2 + FeCI3 + Н2O
6. Для установления соответствия между названием вещества и реагентами, с которыми это вещество может взаимодействовать, необходимо знать свойства этих веществ и определить, с какими реагентами они могут образовывать новые вещества.
- НАЗВАНИЕ ВЕЩЕСТВА:
- A) кальций 1) HBr, N2
- Б) хлорид бария 2) Na2SO4, K3PO4
- В) гидроксид натрия 3) H2O, KOH
- 4) H2SO4, AI(ОН)3
7. Для выбора двух пар веществ, между которыми протекает реакция обмена, необходимо знать, что реакция обмена происходит между двумя элементами, в результате которой атомы одного элемента замещают атомы другого элемента.
Из предложенных пар веществ, между которыми протекает реакция обмена будут:
- 2) оксид бария и гидроксид натрия
- 4) гидроксид алюминия и серная кислота
8. Для вычисления массовой доли железа в нитрате железа(II), необходимо знать состав нитрата железа(II), атомные массы элементов и методику вычисления массовой доли.
9. Для записи молекулярных уравнений реакций, с которых можно осуществить указанные превращения (Ва(OH)2 → X → BaO → BaCI2), необходимо знать состав и свойства реагентов и продуктов, а также знать методику записи химических уравнений.
10. Для вычисления массы образовавшегося осадка при реакции фосфата натрия с хлоридом меди(II) необходимо знать реакционные пропорции и методику вычисления массы вещества. В данном случае, также используется информация о массе и массовой доле фосфата натрия.