Вычислить энергию электрона на разрешенных орбитах и длины волн первых трех линий серии Брэккета (n=4): a) атома водорода
б) иона 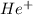
Нарисовать диаграмму уровней

Другие вопросы по теме Физика
Популярные вопросы
- Какой вывод о климате западного и восточного побережий южной америки можно сделать...
3 - 3.44. В треугольнике ABC BC AC АВ. Какой изуглов больше: 1) угол Вили угол А; 2)...
2 - Написать рассказ о жизни греческого мальчика или девочки (50-70 слов)...
2 - 6. Дайын құрылымды толықтырып жаз.уакытта киіктер азайып бара жатыр. МаралдардыңҚазіргі...
3 - Прямоугольный участок земли площадью 60 метров в квадрате обнесен изгородью длина...
3 - Найдите все натуральные значения Х , при котором верно это неравенство.(полное решение...
3 - спочно СОР по русскому честно ...
2 - 8 Вставле подходящие притяжательные местоимения...
2 - 74/25 првратите в десятичную дробь...
2 - Кут між площенами авс і авд 45,авс рівностороній...
1
E = -13.6/n^2
где E - энергия электрона, n - главное квантовое число.
Для атома водорода с n=4:
E = -13.6/4^2
E = -13.6/16
E = -0.85 эВ (электрон-вольт)
Теперь перейдем к определению длин волн первых трех линий серии Брэккета. Длина волны можно найти с использованием формулы Бальмера:
1/λ = R(1/n1^2 - 1/n2^2)
где λ - длина волны, R - постоянная Ридберга, n1 и n2 - главные квантовые числа.
Для атома водорода с n=4 и первой линии серии Брэккета (n1=4 и n2=2), длина волны будет:
1/λ = R(1/4^2 - 1/2^2)
1/λ = R(1/16 - 1/4)
1/λ = R(3/16) (1)
Аналогично вычисляем длины волн для второй (n1=4 и n2=3) и третьей (n1=4 и n2=4) линий серии Брэккета:
Для второй линии:
1/λ' = R(1/4^2 - 1/3^2)
1/λ' = R(1/16 - 1/9)
1/λ' = R(5/144) (2)
Для третьей линии:
1/λ'' = R(1/4^2 - 1/4^2)
1/λ'' = 0 (3)
Таким образом, длины волн первых трех линий серии Брэккета для атома водорода с n=4 будут:
(1) λ = 16R/3 (первая линия),
(2) λ' = 144R/5 (вторая линия) и
(3) λ'' = 0 (третья линия).
Теперь рассмотрим ион гелия He+ (He^+). Для иона He+ нужно учесть изменение заряда ядра атома водорода.
Энергия электрона на разрешенных орбитах иона He+ также вычисляется с использованием формулы Ридберга, но с учетом измененного заряда ядра:
E = -13.6Z^2/n^2
где E - энергия электрона, Z - заряд ядра, n - главное квантовое число.
Для иона He+ с n=4 и Z=2:
E = -13.6(2^2)/4^2
E = -13.6(4)/16
E = -13.6/4
E = -3.4 эВ (электрон-вольт)
Для определения длин волн линий серии Брэккета в случае иона He+ также используем формулу Бальмера, но с учетом измененного заряда ядра:
1/λ = RZ^2(1/n1^2 - 1/n2^2)
где λ - длина волны, R - постоянная Ридберга, Z - заряд ядра, n1 и n2 - главные квантовые числа.
Для иона He+ с n=4 и первой линии серии Брэккета (n1=4 и n2=2), длина волны будет:
1/λ = R(2^2)(1/4^2 - 1/2^2)
1/λ = R(4)(1/16 - 1/4)
1/λ = R(1/4) (4)
Аналогично вычисляем длины волн для второй (n1=4 и n2=3) и третьей (n1=4 и n2=4) линий серии Брэккета:
Для второй линии:
1/λ' = R(2^2)(1/4^2 - 1/3^2)
1/λ' = R(4)(1/16 - 1/9)
1/λ' = R(5/36) (5)
Для третьей линии:
1/λ'' = R(2^2)(1/4^2 - 1/4^2)
1/λ'' = 0 (6)
Таким образом, длины волн первых трех линий серии Брэккета для иона He+ с n=4 будут:
(4) λ = 4R (первая линия),
(5) λ' = 36R/5 (вторая линия) и
(6) λ'' = 0 (третья линия).
На диаграмме уровней, оси OX будет отвечать главное квантовое число n, а по вертикали будут указаны значения энергии электрона. Мы можем отметить энергию электрона на разрешенных орбитах и длины волн первых трех линий серии Брэккета для атома водорода и иона He+ с n=4.