Вобъемом 110 л находится 0,56 кг азота и 1,6 кг кислорода . определить давление смеси газов ппри температуре 27 градусов
Другие вопросы по теме Физика
Популярные вопросы
- іть будь ласка. не можу розібратися!...
2 - Если взвод солдат разбить на бригады по 7 человек, то 2 человека...
3 - Задайте 5 вопросов по содержанию текста...
2 - Дайте развернутый ответ на вопросы: 1.Какой эпизод из сказки «Снегурочка»...
1 - Проблематика твору Суботик повертається в суботу або Машина для...
2 - Дано: угол ВОС- АОС= 18°, угол АОВ=70°, найти угол АОС, угол ВОС...
3 - Спільне і відмінне в державах Індії і Західної Європи за доби СередньовіччяСпільне...
1 - Оқылым материалы бойынша негізгі ойды білдіретін сөйлемдерді іріктей...
1 - АЙТЫЛЫМ 8-тапсырна. Создердi сәйкестендiрiп, сөйлем құрап айт....
1 - , составить алгоритм в питоне Дано Х. Если х3+х2+х+1 не равно 0,...
3
По уравнению Менделеева-Клайпирона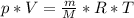 , где р - оказывающее давление (Па), V - объём (м³), m - масса вещества (кг), M - малярная масса вещества (кг/моль), T - абсолютная температура (К). Отсюда выражаем находимое давление:
, где р - оказывающее давление (Па), V - объём (м³), m - масса вещества (кг), M - малярная масса вещества (кг/моль), T - абсолютная температура (К). Отсюда выражаем находимое давление: