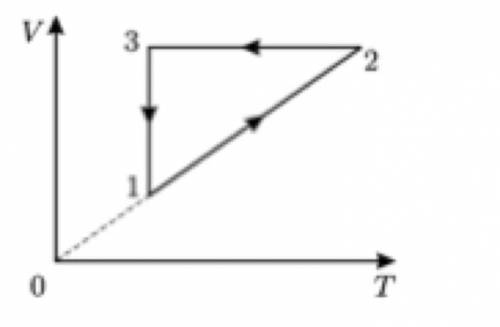
На рисунке представлен циклический процесс, проведенный . идеальным газом в количестве 1 моль а) Дайте название каждого цикла процесса; б) Как изменяются термодинамические параметры газа при переходе из одного состояния в другое?
в)Напишите уравнения, описывающие каждый цикл;
г) Изобразите этот процесс в координатах: p T и V р
Другие вопросы по теме Физика
Популярные вопросы
- Какие слова не образуют словосочетании высокая дерево медленно идет...
2 - Разбирите на : царство , отдел , класс , семейство , род и вид цветок...
3 - Удитячий табір 63 кг яблук в ящиках по 7 кг у кожному й стільки ж...
1 - 30 слов с чердующимися гласными о/а е/и...
3 - Придумать сказку (желательно подлиннее) с присказкой зачином и концовкой....
2 - Синтаксический разбор предложения. какой у нее голос?...
1 - Для большинства млекопитающих характерен признак. 1) трехкамерное...
3 - Назови каждую группу животных одним словом. 1-ая группа- сорока,...
2 - Фонетический разбор фразы семь бед-один ответ...
2 - Запах этот был ее словами слезами и молитвой. слова: словами слезами...
3
1) AB: Изотермическое сжатие;
2) BC: Адиабатическое сжатие;
3) CD: Изотермическое расширение;
4) DA: Адиабатическое расширение.
б) При переходе из одного состояния в другое изменяются термодинамические параметры газа:
1) Во время изотермического процесса температура газа остается постоянной, а давление и объем могут меняться;
2) Во время адиабатического процесса нет теплообмена между газом и окружающей средой, поэтому изменяются как давление, так и объем газа.
в) Уравнения, описывающие каждый цикл:
1) AB: PV = nRT (уравнение состояния идеального газа), где P - давление, V - объем, n - количество вещества, R - универсальная газовая постоянная, T - температура.
2) BC: PV^(γ) = const, где γ - показатель адиабаты, отношение молярных теплоемкостей при постоянном давлении и объеме.
3) CD: PV = nRT.
4) DA: PV^(γ) = const.
г) График в координатах p-T и V-r:
- На графике в координатах p-T газ можно изобразить четырьмя отрезками: AB, BC, CD, DA.
- На графике в координатах V-r можно изобразить цикл в виде замкнутой области, где каждая точка представляет определенное состояние газа в процессе.