Какова масса кислорода содержащегося в объемом 50 л при температуре 27 и давлении 2 мпа
Другие вопросы по теме Физика
Популярные вопросы
- Написать рассказ, который должен содержать 5 фразеологизмов не менее 10 предложений...
2 - Решить (4√3-5)√3+√60 и еще решить √12y-√48y+√3y...
3 - 82-5•8+27: 3 прочитай выражения.найди их значения...
2 - За контрольную работу учащиеся 9 класса получили 6 отметок 5 , 10 отметок 4 , 8...
1 - Постройте график функции y=корень минус х...
2 - Сюжеты и образы первобытных изображений...
2 - Последнее других событий произошло а)объединением италии б)парижская коммуна в)провозглашение...
2 - Точки o и p лежат соответственно на рёбрах ad и cd треугольной пирамиды dabc (рис....
3 - Груз массой 80 кг , лежащий на полу поднимающегося лифта, давит на пол с силой...
3 - При каких значениях a: корнем уравнения (a+3)x-3=a является любое число? ?...
1
Дано:
V=50 л=50*10^-3 кг.
T=27 град Цельсия=300 К.
P=2 МПа=2*10^6 Па.
m=?
________
M=32*10^-3 кг/моль. (Молярная масса кислорода).
________
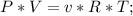
Решение:
Запишем уравнение Менделеева - Клапейрона для данного случая:
Где v - кол-во вещ-ва, формула которой:
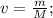
Получаем:
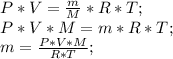
R - универсальная газовая постоянная равная, 8,31 Дж/К*Моль.
Считаем:
m=(2*10^6*50*10^-3*32*10^-3)/(8,31*300)=1,28 кг.
ответ: m=1,28 кг.