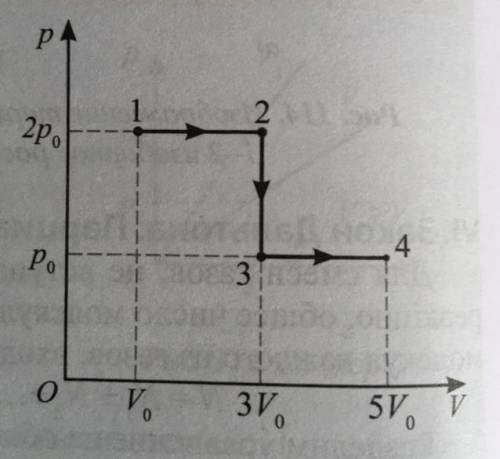
Изобразите на pТ- и VТ-диаграммах процесс, проводимый с идеальным газом (рис 115). Во сколько раз температура газа в состоянии 4 больше температуры в состоянии 1?
Другие вопросы по теме Физика
Популярные вопросы
- 1) 81x^4-18x^3+x^2=0 2) 27t^3+36t^2+12t=0...
2 - Взаповеднике 20000 растений. из них 850 редких. на сколько больше в заповеднике...
2 - Каков характер изменения равнодействующей сил, приложенных к автомобилю, график...
1 - Найти область определения 1)y=√x-12/x^2-16x+48 2)y=x^2-1/x^2-10x...
1 - Профильный ривень 10 клас истер 1.19...
2 - Воктябре 2011 года возраст пелагеи был на 2 больше суммы цифр этого года. сколько...
3 - Сөздері сөз құрамыңыз қарай талдауңыз ,кімдер ,ержүрек ,халық, ң...
1 - 75 это на части или нет? просто ответьте без решения...
3 - Вчесть какого собития отмечается день народного единства?...
1 - Составьте предложение со словом «внимательный-внимание » , в причастном и деепричастном...
3
Из рисунка видно, что в состоянии 1 температура равна Т1 = 200K. А в состоянии 4 она равна Т4 = 800K.
Теперь давайте построим pТ-диаграмму. Для этого нужно знать давление газа в каждом состоянии. На рисунке это указано в виде воображаемых пунктирных линий. Давление в состоянии 1 обозначим p1, а в состоянии 4 - p4.
Так как изображенный процесс проводится с идеальным газом, то в процессе никакая работа или теплота не поглощаются или выделяются. Это означает, что процесс адиабатический и безобъемный.
На рисунке пТ-диаграммы видим, что процесс является горизонтальным, так как объем газа (или V) не меняется, а только меняется температура.
То есть, на pТ-диаграмме, процесс будет изображаться как горизонтальная линия, находящаяся на одном уровне p1 и p4.
Теперь перейдем к VТ-диаграмме. Здесь нужно знать значения объема газа в каждом состоянии. Обозначим их V1 и V4.
На VТ-диаграмме видно, что процесс является изохорическим, то есть объем газа не меняется. Поэтому на VТ-диаграмме процесс будет изображаться как вертикальная линия, проходящая через значения V1 и V4.
Теперь давайте рассчитаем на сколько раз температура в состоянии 4 больше температуры в состоянии 1.
Из условия задачи известно, что Т1 = 200K и Т4 = 800K.
Для определения во сколько раз одно значение больше другого, необходимо разделить большее значение на меньшее:
Т4 / Т1 = 800K / 200K = 4
Таким образом, температура газа в состоянии 4 больше температуры в состоянии 1 в 4 раза.
Итак, ответ на вопрос: в состоянии 4 температура газа больше температуры в состоянии 1 в 4 раза.