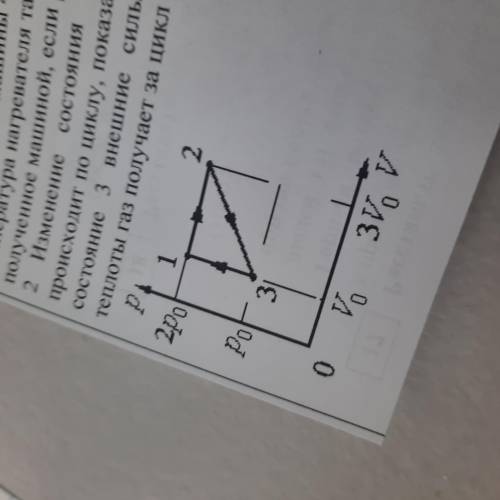
изменение состояния постоянной массы одноатомного идеального газа происходит по циклу, показанному на рисунке. При переходе газа из состояния 2 в состояние 3 внешние силы совершают работу а23 =5кДж. Какое количество теплоты газ получает за цткл от нагревателя?
Другие вопросы по теме Физика
Популярные вопросы
- Что значит рациональное и иррациональное число? примеры...
3 - Какова цель инструкция пользователя компьютера...
2 - Один из смежных углов в 5 раз меньше другого.какая градусная мера большего...
1 - Какая надпись на статуе свободы. что обазначает изоброжение на флаге сша...
2 - Решите ! важно ! : найдите значение выражения 12a-7: b , если a= 1.8 ( простая...
1 - Имеются два одинаковых металлических шарика заряд одного 2*10(в -9 степени)...
3 - Сочинение-рассуждение каждый должен проявлять великодушие сильного и бережливость...
3 - Сложные слова. сложносокращённые слова. ответе на это вопрос...
1 - Смысл сказки маленькая баба-яга смысл сказки чук и гек ответить на любой из...
1 - 824: 7 решить пример в столбик 20...
2
Перейдем к анализу цикла изображенного на рисунке. На рисунке видно, что газ проходит через следующие состояния:
1) Из состояния 1 в состояние 2:
Здесь не указана работа и теплота, поэтому мы не можем использовать эту часть цикла для решения задачи.
2) Из состояния 2 в состояние 3:
Здесь указана работа a23 = 5 кДж, которую совершают внешние силы при переходе газа из состояния 2 в состояние 3.
3) Из состояния 3 в состояние 1:
Здесь не указана работа и теплота, но мы знаем, что цикл является замкнутым, поэтому работа, совершенная внешними силами при этом переходе, должна быть равна противоположной работе, совершенной внешними силами при переходе из состояния 1 в состояние 2.
Теперь мы можем использовать первый закон термодинамики, чтобы найти количество полученной газом теплоты за цикл. Формула будет выглядеть следующим образом:
Q_цкл = W_a23 + W_a31,
где Q_цкл - количество теплоты, полученное газом за цикл,
W_a23 - работа, совершенная внешними силами при переходе газа из состояния 2 в состояние 3,
W_a31 - работа, совершенная внешними силами при переходе газа из состояния 3 в состояние 1.
Мы уже знаем, что W_a23 = 5 кДж. Теперь нам нужно найти W_a31.
Работа, совершенная внешними силами при переходе газа из состояния 3 в состояние 1, равна противоположной работе (W_a23) и она также равна изменению внутренней энергии газа при этом переходе.
Теперь нам нужно доказать, что изменение внутренней энергии газа при переходе из состояния 3 в состояние 1 равно W_a23.
Одноатомный идеальный газ подчиняется уравнению состояния, известному как уравнение Пуассона:
U = (3/2)nRT,
где U - внутренняя энергия газа,
n - количество вещества газа (в молях),
R - универсальная газовая постоянная,
T - температура газа.
Учитывая, что газ остается одним и тем же веществом во всех состояниях цикла, мы можем полагать, что nR является постоянным значением. Таким образом, изменение внутренней энергии газа при переходе из состояния 3 в состояние 1 равно разности внутренних энергий в этих состояниях:
ΔU = U_1 - U_3 = (3/2)nRT_1 - (3/2)nRT_3 = (3/2)nR(T_1 - T_3),
где ΔU - изменение внутренней энергии,
T_1 и T_3 - температуры газа в состояниях 1 и 3 соответственно.
Изнутри изображения на рисунке, мы видим, что температура газа в состоянии 3 выше, чем в состоянии 1 (T_3 > T_1), следовательно, ΔU > 0. Это означает, что изменение внутренней энергии газа при переходе из состояния 3 в состояние 1 положительное и равно W_a23:
ΔU = W_a23.
Теперь мы знаем, что W_a31 = -W_a23 = -5 кДж (работа теплообмена с газом).
Возвращаясь к изначальной формуле:
Q_цкл = W_a23 + W_a31 = 5 кДж + (-5 кДж) = 0.
Таким образом, количество теплоты, которое газ получает за цикл от нагревателя, равно нулю.