я не понимаю как это надо делать
Другие вопросы по теме Химия
Популярные вопросы
- Борьба за светвсе деревья в лесу вместе распространяются вширь...
2 - Изображение животных, в христианстве. сообщение....
3 - Михайло стельмах гуси-лебеді летять план до першого роділу...
3 - Найдите в ниже списке отличительные черты массовой культуры и запишите...
1 - Read the text and fill in the gaps ! with the words from the list....
1 - Читать н.в. гоголь ревизор . образ хлестакова письменно в тетрадях....
2 - Умоляю решите просто умолюя вас ради бога решите вы же умные умоляю...
3 - Your english-speaking pen friend nikki is going to visit you for...
3 - Напишіть рівняння реакцій між речовинами та вкажіть тип хімічного...
2 - Сколько глав было посвященно о жизни мцыри в монастыре? а сколько...
3
Объяснение:
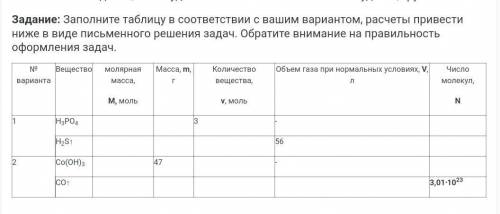
1. Формула: H3PO4 -ортофосфорная кислота, Молярная масса: 98 г/моль
m(H3PO4)=n(H3PO4)*M(H3PO4)=3*98=294г
N=n*Na=3*6.02*10^23 =18.066*10^23 или 1,8066*10^24
Na-постоянная Авогадро 6.022⋅10^23 моль −1.
2.Формула: H₂S - сероводород, Молярная масса: 34 г/моль
n(H2S)=V:Vm=56/22.4=2.5моль
Один моль любого газа при одинаковых температуре и давлении занимает один и тот же объём, при нормальных условиях равный 22.41383 литра. Эта величина известна как молярный объём газа - Vm.
m(H2S)=n(H2S)*M(H2S)= 2.5*34=85г
N(H2S)=n(H2S)*Na=2,5*6.02*10^23 =15.055*10^23 или 1,5055*10^24
3.Формула: - гидроксид кобальта (ІІІ),Молярная масса: 110 г/моль
n(Co(OH)3 )=m(Co(OH)3 ):M(Co(OH)3 )= 47/110=0.427моль
N(Co(OH)3)=n(Co(OH)3)*Na=0.427*6.022*10^23 =2.573*10^23
4.Формула: CO - оксид углерода (ІІ), Молярная масса: 28 г/моль
n(CO )=N(CO )/Na=3.01*10^23/6.02*10^23=0.5моль
m(CO )=n(CO )*M(CO )= 0,5*28=14г
V(CO )=n*Vm=0.5*22.4=11.2л