Выведите молекулярную формулу вещества, содержащего углород ( массовая доля 85,7%) и водород( 14,3%).плотность паров по водороду равно 21
Другие вопросы по теме Химия
Популярные вопросы
- «Күлтегін» жырындағы «Осы бір түркі елі ел болсын деп, бастаған ісіміз...
1 - Бунақденелілердің пайдасы мен зичны...
1 - VI-IX ғасырларда түрік тайпаларының көші-қон үдерісінің кеңеюіне не ықпал...
3 - 1.Матеріальна точка рівномірно обертається по колу радіусом 9 м, здійснюючи...
3 - Определите, какие утверждения являются «верными», и какие «неверными»....
2 - Определите аналитически и графически: 1. Рановесные цену и объем продажУсловие:...
2 - Вынося общий множитель за скобки,найдите значение выражения: а)57*19+43*19б)36*78+49*35+64*78-29*35...
2 - Почему число 98*25 делится на 35...
2 - 2. Почему Сулайманова и Исабеков - герои произведений Ч. Айтматова - испытывают...
3 - ответьте на задание своими словами. В одном из сочиненний К.Маркса и Ф.Энгельса,...
2
Я покажу еще один решения этой задачи, он немного проще.
Рассчитаем молекулярную массу вещества, через плотность по водороду:
Mr = D*2 = 21*2 = 42
Колиечтва атомов водорода и углерода рассчитаем используя их массовые доли.
Пусть формула неизвестного вещества -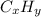
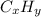
Атомная масса углерода в этом соединении: 12*х
Атомная масса водорода в этом соединении: y
Получаем 12х+у=42
Запишем формулу для получения массовой доли углерода:
Подставим изестные велечины - массовая доля угдерода - 85,7% или 0,857 и молекулярную массу - 42:
Находим икс:
х = 0,857*42/12 = 3
Из молекулярной массы УВ вычтем атомную массу 3 атомов углерода(их мы установили, что три):
42 - 36 = 6
6 - это и есть число атомов водорода
C3H6
Расчет ведем на 100 г вещества.
ν (С) = 85,7/12 = 7,14 моль атомов С
ν (Н) = 14,3/1 = 14,3 моль атомов Н
ν (С) :ν (Н) = 1:2
М (СхHy) = 2·21 = 42 г/моль
Формула вещества, исходя из полученного соотношения атомов С и Н: СnH2n
Cоставляем уравнение:
12·n + 1·2n = 42
14n = 42 ; находим n = 3 Следовательно, формула вещества С3Н6