Вычислить массу соли и объем водорода который выделится при взаимодействии алюминия и хлоридной кислоты массой 73 г распишите дано и решение
Другие вопросы по теме Химия
Популярные вопросы
- Найдите число m если 9/11 от м составляет 60% от 45...
2 - Выполните морфологический разбор выделенных слов :Это з…ставило¹ задумат…ся о...
1 - Визначити проблему яка порушується гумореска А) ПохвалаБ) ЕволюціяВ) Найважча...
2 - Сформировать и вывести на экран последовательность из 1 =n =90 элементов, заданных...
1 - Найдите область определения...
2 - Найдите значение выражения 0,4*(-10)^3-7*(-10)^2+64 Полное решение нужно...
1 - составить по плану описание Камчатки...
3 - Укажіть природну зону, де розміщено найбільше виноробних заводів україни А-Мішаних...
1 - Схемі [...], (...), [...], (...) відповідає речення Вибалок затоплено різнотрав...
1 - Log1/2 (2x-1)/(16-x^2) 2...
2
Дано: РЕШЕНИЕ 2Al+6HCl=>2AlCl3+3H2
m(HCl)=73г n(AlCl)=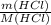 =
=
Найти: m(AlCl)![\frac{73 }{36} = 2.03 моль.V(Н2) Находим n(AlCl) Составляет пропорции.[tex]x=\frac{2.03*2}{6}](/tpl/images/0942/1156/4f893.png) =0.68 моль.
=0.68 моль.
m=M*n=132*0.68=89.76 г
V(H2)=Vm*n
n(H2O)=ЧЕРЕЗ ПРОПОРЦИИ=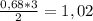
V(H2)=Vm*n=22.4дм3/моль*1,02моль=22,8дм3.