Вот здесь есть , решите их и я выберу ваш ответ лучшим. 1.напищите уравнения электролитической диссоциации для следующих веществ: baci 2 , k 2co3 , ba(oh)2 2.осуществить следующее превращение: сo2 уравнения запишите в молекулярном, полном и сокращенном ионном виде. 3.подберите такие вещества взаимодействие между которыми выражалось сокращенным ионным уравнением типа: 2h + s 4.cколько граммов водорода выделится при взаимодействии магния с 98г 20% раствора серной кислоты?
Другие вопросы по теме Химия
Популярные вопросы
- Вромбе abcd, ao=2bo. найдите периметр ромба, если его площадь равна...
1 - (5) определите координаты сто-лицы нашей родины...
1 - Рассказ о учёном по окружающему миру 3 класс...
3 - Складіть діалог для чого потрібен інтернет ? ( 8-10реплік ) і запишіть...
3 - Температура тела в зависимости от времени задается формулой t=0,3t²(t-...
1 - Найти площадь параллелограмма....
1 - 1) представляет собой систему обозначений и правил предназначенную...
2 - 15 - подготовить ообщение на тему: передачи и броски в баскетболе...
3 - Расставьте запятые. в каком (каких) из примеров количество частей...
3 - Вставьте пропущенные слова заранее )...
2
1)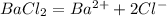
2) CO2 + H2O = H2CO3
H2CO3 + Ba(OH)2 = BaCO3 + 2H2O
3) H2SO4 + Na2S = H2S + Na2SO4
4) Mg + H2SO4 = MgSO4 + H2
Рассчитаем массу кислоты в растворе:
m(р.в.) = W*m(р-ра) = 0,2*98г = 19,6г
Рассчитаем количество вещества кислоты:
n = m/M = 19,6г/98г/моль = 0,2моль
По уравнению реакции:
n(H2) = n(H2SO4) = 0.2моль
Рассчитаем массу водорода:
m = n*M = 0,2моль*2г/моль = 0,4г