Влияние различных факторов на скорость химической реакции. Цель: рассмотреть влияние различных факторов на скорость химической реакции.
Оборудование и реактивы: пробирки, спиртовка, держатель, штатив для пробирок, цинк, магний,
железо: гранулы и порошок, растворы серной (1:5, 1:10) и соляной кислоты, пероксид водорода, оксид
марганца(IV), оксид мед (II).
Ход работы:
ОПЫТ 1. Влияние природы реагирующих веществ.
Налейте в три пробирки по 2 мл раствора соляной кислоты. Положите в первый стакан кусочек магния,
во второй стакан - гранулу цинка, в третий – кусочек железа. Наблюдайте скорость трех
реакций. Какая из реакций самая быстрая и почему?
ОПЫТ 2. Влияние концентрации реагирующих веществ.
В две пробирки, наклонив их, опустите по грануле цинка, осторожно прилейте растворы серной
кислоты: в первую пробирку раствор кислоты 1:5, во вторую – 1:10. В какой из них реакция идет
быстрее?
ОПЫТ 3. Влияние площади соприкосновения реагирующих веществ.
В одну пробирку насыпьте немного порошка железа, в другую – положите железную скрепку и в обе
пробирки прилить по 2 мл разбавленной соляной кислоты (1:2). В какой из пробирок реакция идет
быстрее? Почему?
ОПЫТ 4. Влияние температуры.
В две пробирки поместите немного черного порошка оксида меди (II), прилейте в обе пробирки раствор
серной кислоты. Одну из пробирок нагрейте. В какой из пробирок реакция идет быстрее? Почему?
ОПЫТ 5. Влияние катализатора.
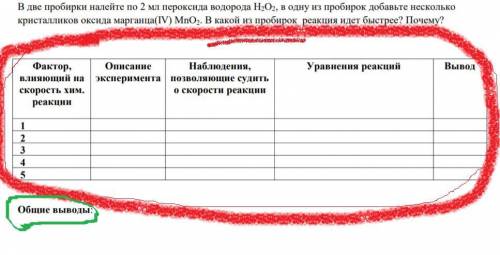
В две пробирки налейте по 2 мл пероксида водорода Н2О2, в одну из пробирок добавьте несколько
кристалликов оксида марганца(IV) MnO2. В какой из пробирок реакция идет быстрее? Почему?
После этого:
Ответы
Показать ответы (3)
Другие вопросы по теме Химия
Популярные вопросы
- УМОЛЯЮ СДЕЛАЙТЕ ПЕРЕСКАЗ SpringSt David s Day. March 1st is a very important...
2 - Составить химическое уравнение...
2 - Какой бы я поставил памятник петру1...
1 - Верно ли высказывание (ответьте «да» или «нет»): 7. Если упростить выражение...
3 - Задание 1. Укажите исторические изменения структурного характера /опрощение;...
3 - Сеня и Саша играют в игру «крестики-крестики». Игра заключается в том, что Сеня...
1 - Суспільно-політичні течії країн Заходу першої половини 19 ст(табл) Перша колонка:...
2 - Choose the correct item:1. “Excuse me, do you know where the supermarket is?”“Yes,...
3 - 18. Рассмотрите этапы в жизненном цикле насекомого. Дайте ответы на вопросы.1....
3 - Переведите если Переведёте бан...
3