В порции кислорода объемом 4,48 см³ или озона массой 9,60 мг содержится больше атомов? ответ подтвердите расчётами.
Другие вопросы по теме Химия
Популярные вопросы
- Решите опредилить начальную скорость ускорения, написать уравнение...
1 - Решите , техническая механика...
1 - Для детей какого возраста фильм бегущий в лабиринте 2 и 3 (+6...
1 - Гипотенуза прямоугольного треугльника равна 20 см один из катетов...
1 - Ксложным веществам относятся: а)кислород б) азот в) вода г) сера?...
1 - Найдите отношение длин окружностейи площадей двух кругов, если...
1 - Всаду размерами 30х41 целая 2/3 хотят сделать трапинку шириной...
3 - Сделайте сор с дано и решением с рисунком обязательно...
3 - 1. вычисли количество сернистого газа so2, в котором содержится...
1 - 6. на столе лежит стопка карт вверх. требуется переложить их в...
2
В порции озона. 3,6*10^20 против 2,4*10^13.
Объяснение:
Итак, основная формула - применяемая в этой задаче
N =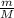 *Na, Na - число Авогадро, равное 6,022*10^23 моль⁻1, а N - число молекул
*Na, Na - число Авогадро, равное 6,022*10^23 моль⁻1, а N - число молекул
Для озона все проще - 0,0096 г/46 г/моль * 6,022*10^23 моль⁻1, ≈ 1,2044*10^20
Для кислорода все на шаг дольше, поскольку дан объем, а не масса. Эти две величины связаны соотношением V =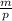 , отсюда m = V*p
, отсюда m = V*p
N =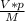 *Na = (0,00000448 м^3* 0,00143 г/м^3) * 6,022*10^23 моль⁻1, /32 г/моль ≈ 1,2056*10^13
*Na = (0,00000448 м^3* 0,00143 г/м^3) * 6,022*10^23 моль⁻1, /32 г/моль ≈ 1,2056*10^13
В молекуле озона - три атома, кислорода - два атома. 3,6*10^20 против 2,4*10^13. Очевидно, в данной порции озона атомов больше, чем в данной порции кислорода.
Я не применял формулу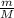 =
= 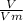 ; поскольку не указаны условия, а известное в пособиях значение константы Vm применяем для нормальных условий.
; поскольку не указаны условия, а известное в пособиях значение константы Vm применяем для нормальных условий.