Составить уравнения окислительно-восстановительных реакций методом электронного (указать степени окисления элементов, число отданных и принятых электронов и т.д). : ) 1) k+br2=kbr2 2) 3ba+n2=ba3n2 3) mg+h2so4(разб.)=mgso4+h2 4) 2li+2h2o=2lioh+h2
Другие вопросы по теме Химия
Популярные вопросы
- Строительная отрасль кыргызстана...
1 - Охарактеризувати сузір я, як одиницю всесвіту...
2 - 2. С какими странами взаимодействовала Россия? 3. Главная задача внешней политики...
1 - 6.Что мешает любви главных героев? 7.Кто такой Тибальт? Как он погиб? 8.Как...
3 - Задание: Построить графики функций. Провести исследование по плану:а) область...
2 - Укажите ряд, в котором на месте всех пропусков пишется одна и та же буква...
1 - Сөйлемдегі жылдарды ғасырға айналдыр......
3 - Как переводится birthday summer solstice? ...
2 - Вставь пропущенные буквы. Расставь знаки препинания при причастных оборотах....
1 - Установи соответствия ,кому из героев сколько было лет: автор- пани Ядя- Ткачук-...
2
0 0 +1 -1
1)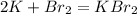
0 +1
K -1e = K |2|восстановитель(окисление)
0 -1
Br2 + 2e = 2Br |1|окислитель(восстановление)
0 0 +2 -3
2)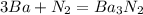
0 +2
Ba - 2e = Ba |3|восстановитель(окисление)
0 -3
N2 + 6e = 2N |1|окислитель(восстановление)
0 +1 +2 0
3)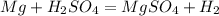
0 +2
Mg -2e = Mg |1|восстановитель(окисление)
+1 0
2H +2e = H2 |1|окислитель(восстановление)
0 +1 +1 0
4)
0 +1
Li - 1e = Li |2|восстановитель(окисление)
+1 0
2H + 2e = H2 |1|окислитель(восстановление)