Сколько граммов кристаллогидрата CaCl2⋅6H2O надо добавить к 350 г 10%-го раствора CaCl2, чтобы удвоить массовую долю хлорида кальция в растворе? ответ округлите до целого числа.
Другие вопросы по теме Химия
Популярные вопросы
- Постройка дома стоит 382 200 руб. за этой суммы по 45% приходится на стоимость...
2 - Для каждого значения параметра а решите уравнение (a-2)x=...
1 - Какая пословица в рассказе выскочка м.м. пришвин...
3 - Решите столбиком 329+408900\174-327*74...
3 - Запиши числа в порядке убывания 10 3385 , 8 003 , 13 368 , 275 , 102 030...
3 - Напишите уравнение реакций соответствующих превращениям mno2- mn- mn(no3)2-...
3 - Горесть - это глагол или существительное?...
1 - Написать сочинение на тему: наводнение 5класс...
3 - Если к шарику заряженного электрометра поднести руку (не касаясь шарика,...
1 - Переведите ! it is not the first time linda s father is walking down the...
3
114,0625 г
Объяснение:
Пусть n(CaCl2⋅6H2O) = x моль, тогда:
m(CaCl₂) = 111x г
m(H₂O) = 108x г
m(CaCl2⋅6H2O) = 219x г
Теперь перейдём к раствору:
m(CaCl₂) = 350 * 0,1 = 35 г
m(исходного раствора CaCl₂) = 350 г
Нам надо довести массовую долю соли до 20%
(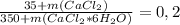
67,2x = 35
x = 0,5208333333 моль
m(CaCl2⋅6H2O) = 219 г/моль * 0,5208333333 моль = 114,0625 г