разобрать реакции методом электронного баланса. ( окислитель, восстановитель) Заранее
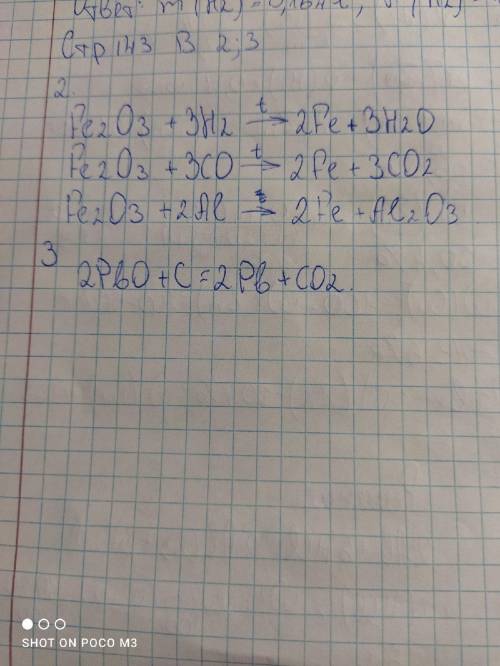
Другие вопросы по теме Химия
Популярные вопросы
- 1.ключевые слова2.ваше отношение к мари и щелкунчику3.как автор относится...
1 - Желательное полное решение. предмет, высота которого равна 13 см, расположен...
1 - Краствору серной кислоты добавить хлорид бария ( bacl2) составить уравнение...
1 - На сторонах угла q отложены равные отрезки qr и qp. через точки р и r проведённа...
1 - Визначити молекулярну формулу вуглеводню який містить 86% карбону відносна...
1 - complete the sentences. use the past simpleand the past continuous in each...
2 - Написать сочинение на тему злодеяние и возмездие...
1 - Сочинение на любую тему с не с сказуемыми == их должно быть минимум штук 15...
3 - Chap ustunda berilgan iboralarning mazmunini onq ustunga yozing yeng ichida...
2 - Какой объем займёт 400г гелия при температуре 25 градусов и давлении 120 кпа....
3
Объяснение:
привет :з
для того, чтобы расставлять коэффициенты при метода электронного баланса, следует знать несколько правил и уметь правильно расставлять степени окисления.
Какие должны быть знания относительного самого метода:
например, Fe (+3) говорит о том, что у железа не хватает 3 электрона, если O (-2), то у него в избытке 2 электрона; у отдельно стоящих элементов (например, Н2) степень окисления равна 0, это говорит о том, что электроны в достатке.
окислитель - тот, кто принимает электроны, восстановитель - тот, кто отдаёт. окисление - отдача электронов, восстановление - принятие электронов.
Алгоритм расстановки:
1. Сначала расставляем степени окисления над элементами;
2. Ищем те, у кого меняются степени окисления слева направо;
3. Дальше используем знания, которые я написала выше (+ не хватает, - в избытке, 0 достаточно);
4. Ищем общее кратное и делим на количество электронов;
5. Расставляем коэффициенты в уравнении рядом с теми элементами, у которых общее кратное разделили на количество электронов.
(Примечание: в данном случае у железа можно и обычным поставить коэффициент, поэтому методом электронного баланса не стала)