При крекинге алкана образовались два углеводорода с одинаковым числом атомов углерода. Плотность одного из них составляет 2,589 г/л (н. у.), а массовая доля углерода в нем равна 82,76 Установите молекулярную формулу исходного углеводорода, напишите уравнение реакции крекинга. Напишите уравнение синтеза данного углеводорода по реакции Фишера--Тропша
Другие вопросы по теме Химия
Популярные вопросы
- Определи род имен существительных в каждой группе подчеркни лишнее слово А) медведь...
1 - Https://www.union-bulletin.com/calendar/other/full-watch-da-5-bloods-2020-online-for-free-123movies/event_a01686ac-b371-11ea-a466-5cb9017b8d1b.html...
3 - Нужно ответить на вопросы. 1)Корни, найденные при решении логарифмического уравнения...
2 - Найти наибольшее и наименьшее значение функции y=x^3-6x^2+9 на отрезке [-4;0]...
2 - Даны целое числа m и n.Какое из нижеследующих высказываний о событиях неверно?С...
1 - Сөзді құрастыр: 1)мей-2)құр-3)атқ-4)фак-5)өсі-6)пис-7)тел-8)шаш-9)тұр-10)топ-11)пил-12)ұша-13)ада-...
2 - Решите правильно очень надо вопрос жизни...
3 - В цилиндрический сосуд налили 2100 см3 воды. Уровень воды при этом достигает...
3 - ПРЕ РЕШИТЕ ХОТЬ ЧТО-ТО ИЗ ЗАДАЧ (тесты не надо...
3 - Выполить тест, с решением :...
2
С₈Н₁₈
Объяснение:
При крекинге алканов образуются новые алканы и алкены
Если есть плотность одного из продуктов, то можем (при условии что это газ) посчитать его молярную массу
M(газа) = ρ · Vm = 2.589 · 22.4 = 58 г/моль
Пусть формула образовавшегося вещества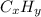 . Напишем следующее соотношение
. Напишем следующее соотношение
Простейшая формула соединения - C₂H₅ с молярной массой 29 г/моль, а реальная молярная масса 58 г/моль, поэтому истинная формула соединения - С₄Н₁₀ - бутан. Значит второй углеводород был бутен. Исходное вещество было алканом и имело 8 атомов углерода. Это был октан - С₈Н₁₈
Пишем реакцию крекинга
С₈Н₁₈ = С₄Н₁₀ + С₄Н₈
Пишем реакцию синтеза октана по Фишеру-Тропшу
8CO + 17H₂ = С₈Н₁₈ + 8H₂O