Предельный одноатомный спирт массой 1,48г,содержащий 64,86% углерода, сожгли в избытке кислорода.образовавшуюся смесь газов пропустили через 200мл раствора кон с массовой долей 5%(плотность1,04г/мл).какая соль образовалась и какова ее масса? напишите структурные формулы всех изомеров исходного спирта и назовите из по международной номенклатуре.
Другие вопросы по теме Химия
Популярные вопросы
- Сколько можно написать двузначных чисел, сумма десятков и единиц которых равна...
1 - Вдень автобус ездиет 30 км , на 100 км автобус берет 9 литров бензина. сколько...
1 - За 3 часа работы экскаватор вынул 555 м3 земли сколько кубических метров вылет...
1 - Мотоциклист ехал 3 часа со скоростью 48 км ч потом 2 часа со скоростью 54 км...
3 - Постройте график уравнения: 3x-y+2=0...
3 - Из группы однокоренных слов выпиши слова с безударным гласным в корне. выдели...
1 - What is friendship? что такое дружба? ответ на ....
3 - Синтаксический разбор предложения. много народных пословиц учит нас надеяться...
2 - Найдите соответствия между названием вещества и его формула название вещества...
3 - Будь ласка тре зробити таблицю про навчання в стародавньому єгипті і навчання...
2
Давайте обозначим неизвестный спирт как: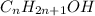
Запишем уравнения протекающих реакций:
У нас известна массовая доля углерода в соединении, давайте попробуем вытянуть из нее
число атомов углерода. Мы знаем, что молекулярная масса равняется сумме атомных масс элементов, для нашего спирта "мистер ИКС" она выглядит вот так: 14n + 18, это уравнение справедливо для всей предельных одноатомных спиртов.
Распишем получение массовой доли углерода:
9.0846n + 11.6748 = 12n - видим, что получилось уравнение с одним неизвестным, причем простое, линенйное. Округлим его.
9n + 12 = 12n, сократим на 3
3n + 4 = 4n
отсюда n= 4 , значит спирт имеет вот такуб формулу:
Запишем уравнение горения:
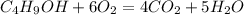
Рассчитаем количество вещества спирта:
n = m/M = 1,48г/74г/моль = 0,02моль
По уравнению реакции:
n(CO2) = 4n(C4H9OH) = 0,02моль*4 = 0,08моль
Теперь, разберемся со второй реакцией, с едким кали:
CO2 + KOH =
Мы не можем предсказать какие точно будут продукты, тут возможны два варианта, либо карбонат калия, либо гидрокарбонат, зависит от того в избытке дана щелочь или нет.
Рассчитаем количество вещества щелочи.
Я сразу нашел количество вещества, в числителе я умножил плотность на объем и на массовую долю, таким образом нашел массу KOH в растворе, а затем разделил на его молярную массу.
Видим, что n(CO2) = 0,08 моль, а n(KOH) = 0,26 моль, значит, CO2 - в недостатке и образуется карбонат калия, пишем уравнение:
CO2 + 2KOH = K2CO3 + H2O
Рассчитаем массу соли.
По уравнению реакции:
n(K2CO3) = n(CO2) = 0,08моль
Рассчитаем массу:
m = n*M = 0,08моль*202г/моль = 16,16г
Изомеры:
CH3 - CH2 - CH2 - CH2 - OH - н - бутиловый спирт(бутанол - 1)
CH3 - CH - CH2 - OH 3 - метилпропанол - 1
|
CH3
CH3 - CH2 - CH - OH 2 - метилпропанол - 1
|
CH3
CH3 - CH2 - CH - CH3 бутанол - 2
|
OH
CH3
|
CH3 - C - CH3 2 метил - пропанол - 2
|
OH
CH3 - O - CH2 - CH2 - CH3 метилпропиловый эфир
СH3 - CH2 - O - CH2 - CH3 диэтиловый эфир
CH3 - CH2 - CH2 - O - CH3 пропилметиловый эфир