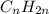Определите молекулярную формулу вещества, при сжигании 2,1г которого получили 6,6г углекислого газа и 2,7г воды. плотность паров его по воздуху 2,9. к какому классу относится данное соединение
Другие вопросы по теме Химия
Популярные вопросы
- Рассчитайте массовую долю кислоты в р-ре полученном после добавления...
2 - Просклонять северный олень сияние звезда...
1 - Оракшы,койшы соз курамына талдау керек...
2 - Придумай несколько верных и неверных высказываний. только смешные!...
2 - Сочинение на тему характеристики жилина и костылина ....
2 - 100б 2500000\500*(3784\3784+0*-703)\29+80*2000...
3 - Последовательность задана формулой =-2+3*n.найдите b...
2 - Картинку животного и от его имени составить рассказ на анг. языке не...
3 - Задать вопрос к словосочетанию: звонили по телефону. звонили (вопрос?...
2 - Как екатерина 1 пришла на власть краткий сообщение...
2
1.Сначала найдем через относительную плотность молекулярную массу вещества:
2.Теперь найдем массы Углерода и Водорода за массами продуктов горения:
а)масса Углерода:
44 г углекислого газа содержит 12 г Углерода,а
6,6 г________________________х г, откуда х=6,6*12/44=1,8 г
б)масса Водорода:
18 г воды содержит 2 г Водорода,а
2,7 г_____________у г, откуда у=2*2,7/18=0,3 г
3.Если сложить полученные массы,то получится 2,1 г,значит это углеводород.так как действительно состоит из атомов Водорода и Углерода(если бы этой суммы не хватало бы,то разница между массой вещества и этими двумя массами элементов,дало бы массу третьего элемента,Кислорода,это на будущее).Теперь поделив каждую массу элемента на массу всего вещества,получим массовые доли этих элементов:
w(C)=1,8/2,1=0,8571 или 85,71%
w(H)=100% - w(C)=100 - 85,71=14,29%
4.Теперь осталось найти количество атомов каждого из элементов в веществе.Для этого необходимо вспомнить формулу по определению массовой доли элемента в веществе и вывести из нее n:
n(C)=Mr(CxHy)*w(C)/Ar(C)*100%=84,1*85,71/12*100=6
n(H)=Mr(CxHy)*w(H)/Ar(H)*100%=84,1*14,29/1*100=12
Вот и выходит,что формула углеводорода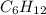 -это гексен - представитель непредельных углеводородов ряда этилена,так как подходит под общую формулу
-это гексен - представитель непредельных углеводородов ряда этилена,так как подходит под общую формулу