Найти массу газа полученного на аноде при электролизе 900 грамм 365 раствора нитрата серебра
Другие вопросы по теме Химия
Популярные вопросы
- Придумайте 10 предложений с порядковыми числительными на языке...
3 - Олег решил навестить своего друга.он вышел из дома и пошел со скоростью...
3 - Хелп ми . 1.высота ромба вместе с диагональю ромба, у которых общая конечная...
1 - Ть побудувати графік функціі...
3 - лексико- граматичеслие котегории этих слов.следы-цаплю-от волка -муравей-сеть-голубка-окном-снег...
3 - Пшеницей засеяли 221 гектаров, что составляет 65 % от всего поля. чему...
2 - Даны плотность газа 1,96 г/л и его элементный состав: углерод и кислород....
2 - Нет опаснее человека,которому чуждо человеческое, который равнодушен к...
1 - Вкаком рассказе художественной человек трудиться чтобы отдыхать? ...
2 - Когда возникла симметрия? желательно побыстрее?...
3
- Электролиз раствора:
K(-):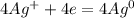
An(+):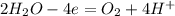
- Рассчитаем массу расворенного вещества соли:
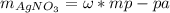 = 900г*0,36 = 324 грамм
= 900г*0,36 = 324 грамм
- Рассчитаем количество вещества соли:
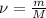 = 324 грамм/170г/моль = 1,9 моль
= 324 грамм/170г/моль = 1,9 моль
- По уравнению реакции:
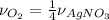 = 1,9моль/4 = 0,476моль
= 1,9моль/4 = 0,476моль
- Рассчитаем массу кислорода:
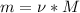 = 0,476моль*32г/моль = 15,232 грамм
= 0,476моль*32г/моль = 15,232 грамм