Кто понимает, 2. составьте схему строения атома хлора. укажите общее число и число неспаренных электронов. запишите формулы типичных соединений. 4.составьте уравнение реакции, расставьте коэффициенты с электронного . укажите окислитель и восстановитель. kвr + сl2 kсl + вr2 6. составьте два уравнения реакций: а) соединения; б) замещения, в которых участвуют галогены. 8. составьте уравнения реакций, позволяющих характеризовать свойства соляной кислоты или других галогеноводородных кислот. 9. вычислите объемы хлора и водорода (н. необходимых для получения 20 м3 хлороводорода.
Другие вопросы по теме Химия
Популярные вопросы
- Хімія 8 клас. Йонний зв язок....
2 - 837. Берілген теңдеулерді шешіп, әлемнің жеті кереметі тураг біздің заманымызтеңдеулерінің...
3 - Заполните таблицу по 1-му действию комедии ...
1 - Быр айнымалысы бар сызықтық теңдеу. Мәндес теңдеулер.Быр айнымалысы бар сызықтық...
3 - 6 сынып математика білім лэндтағы...
3 - Міндо стеа сурын суретке кара Матіне туралы етуі орые Болжап айтАң аулауКеше...
2 - Компактну речовину це що теке...
1 - Напишите эссе на тему считаете ли вы что индустриализация принесла пользу для...
2 - 10. 10. 1) к следующим выражениям подберите синонимичные и составьтеокружающую...
3 - Закінчіть рівняння реакції та вкажіть суму коефіцієнтів перед формулою відновника:Al...
2
2) +17 ) ) )
2 8 7
Общее число электронов: 17
Неспаренных: 1
Хараткреные соединения:
NaCl, HCl
4) 2KBr + Cl2 = 2KCl + Br2
восстановитель: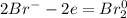 - окисление
- окисление
окислитель: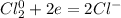 - восстановление
- восстановление
6) а. 5Cl2 + 2P = 2PCl5
б. Cl2 + 2KBr = 2KCl + Br2
8) а. 2HCl + CuO = CuCl2 + H2O
б. 2HCl + Zn = ZnCl2 + H2
в. HCl + AgNO3 = AgCl+ HNO3
г. NaOH + HCl = NaCl + H2O
9) Cl2 + H2 = 2HCl
По уравнению реакции:
V(H2) = V(Cl2) = 1/2V(HCl) = 10м3
ответ: 10м3 - H2,10м3 - Cl2
2)Заряд атома хлора = его порядковому номеру =17
Электронная формула:
Сl +17 .. ) .. ) .. )
2 .. 8 .. 7
1s2 2s2 2p6 3s2 3p5, неспаренный 1 электрон
Типичные соединения:HCl, Cl2O7,NaCl
4) 2KВr + Сl2 = 2KСl + Вr2
Br(-1) -1e = Br2(0) восстановитель
Cl2(0) +1e=Cl(-1) окислитель
то есть перед Br2 и Cl2 ничего не стоит, остальное расставляем так
6) замещения: Cl2 + 2HBr → 2HCl + Br2
соединения: 2Al + 3F2 = 2AlF3
8) 2Na + 2HCl = 2NaCl + H2
MgO + 2HCl = MaCl2 + 2H2O
Al(OH)3 + 3HCl = AlCl3 + 3H2O
2HCl + Na2CO3 = 2NaCl + CO2 + H2O
20м3
9) H2 + Cl2 = 2HCl
1моль 1 моль 2 моль
HCl в 2 раза больше, чем H2 и Cl2, значит и объёма в 2 раза больше. Получается 10м3 H2 и 10м3 Cl2