Какой объем займут 5 кмоль Cl2 ?
Другие вопросы по теме Химия
Популярные вопросы
- Из москвы и саратова вышли одновременно навстречу друг другу два поезда...
2 - Хвост мартышки имеет 60 см. а у гамадрила 20 см. на сколько длиннее...
2 - Скажите какая будет из них идти 1-ая 2-ая и д.т (240: 8-30): 2+(561:...
2 - Идёт числовой ряд 2,5,11,23, что на месте...
2 - He s getting with every day 1)more weaker 2)too weaker 3)so weaker 4)much...
1 - Составьте два предложения : одно-с однородными подлежащими , второе-с...
1 - Напишите уравнения реакций, при которых можно исходя их карбида кальция...
1 - P(b)/p(1/b) при p(b)=(b+6/b)(6b+1/b)...
2 - Перевод в спортлайте 8 класс стр 42 animals in the air...
1 - Почему в египте возник миф о воскресшем боге?...
1
V=112 м^3
Объяснение:
Любой газ n молей при нормальных условия (0 градусов цельсия и атмосферное давление 101300 Па, в задачах часто пишут н. у.) занимает объём V равный:
где Vm - молярный объём равный - Vm=22.4 дм^3
Следовательно 5 кмолей хлора займут объём:
Это и есть ответ :)
Немного теории из физики.
Если условия "не нормальные" (повышенное или пониженное давление или температура), то можно из уравнения Клапейрона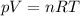 (где T - температура в градусах Кельвина, p - атмосферное давление, n - количество молей, R - универсальная газовая постоянная) найти какой объём занимает тот или иной газ. И как раз если подставить n=1 моль, p=101300 Па, T=273.15К (0 градусов по цельсию), то получиться тот самый молярный объём:
(где T - температура в градусах Кельвина, p - атмосферное давление, n - количество молей, R - универсальная газовая постоянная) найти какой объём занимает тот или иной газ. И как раз если подставить n=1 моль, p=101300 Па, T=273.15К (0 градусов по цельсию), то получиться тот самый молярный объём: