(8 класс)
сера образует два оксида формулы которых so2 и so3. назовите оксиды. в каком из них содержание серы больше? ответ подтвердите расчётами.
Другие вопросы по теме Химия
Популярные вопросы
- Сравнить Есенина с Пастернаком с диаграммой Венна...
2 - нужно найти арифметическое число дроби3-2/5*3 1/3 и...
3 - Решите 1)C est ... rue a Lyon (un) (une) (...) 2)Ce sont ... amis de Michele....
2 - Укажите причину возникновения искры между шариками в вибраторе Герца установленным...
1 - Используя рисунок определи угрозы растительному и животному миру предложи...
1 - Вам по группе объявили о замене на 2 пару. Для студентов вашей группы...
2 - I don t have a sister. I don t have a brother… Укажите правильный вариант...
2 - Очень надо 15 синут осталось...
3 - 2. Приведены некоторые свойства меди: хороший проводник электричества,...
3 - Какое будет условие у задачи номер 9 ...
3
Номенклатура оксидов такая :
Сначала говорим слово "оксид", а потом элемент, образующий оксид, в родительном падеже. Если элемент, образующий оксид, проявляет в соединениях переменную валентность, то в скобках обязательно указываем его валентность римскими цифрами.
SO₂.
Определим валентность серы.
Соединение бинарное, валентность кислорода мы знаем - она постоянна и равна 2.
В бинарном соединении произведение валентности элемента на его индекс равно произведению валентности другого элемента на его индекс.Обозначим валентность серы за х.
Тогда :
x II
SO₂
x = 2*2
x = 4.
Валентность серы равна 4, тогда название SO₂ - оксид серы (IV).
Аналогично и с SO₃.
x II
SO₃
х = 2*3
х = 6.
Тогда SO₃ - оксид серы (VI).
№2.Массовая доля химического элемента в соединении - это отношение относительной атомной массы химического элемента, умноженной на количество её атомов, к относительной молекулярной/формульной массе всего соединения.В SO₂ :
ω(S) =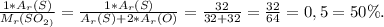
В SO₃ :
ω(S) =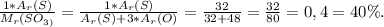
Делаем вывод, что в SO₂ содержание серы больше, поэтому в ответ указываем этот оксид.
ответ : оксид серы (IV) - SO₂.