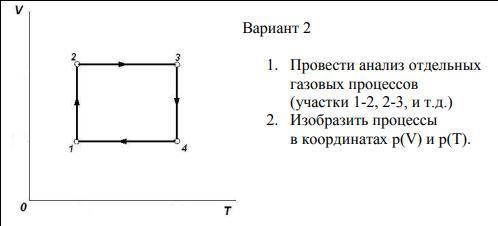
решить! 1). Назвать процессы и указать законы, их описывающие, показать изменения макропараметров газа. 2). Начертить графики изменения состояния газа в координатах pOV и VOT.
Другие вопросы по теме Физика
Популярные вопросы
- Решить кластер,указав верное утверждение,относительно дополнения1)отвечает...
3 - В одном из предложений допущена ошибка. Исправь её. Мама сидела,...
1 - Напишите подробный план по статье Начальное представление о романтизме...
3 - 2. Виберіть назву речовини, структурна формула якої CH3-C=-C-CH,Cl:А...
3 - 5. Вычислите, используя распределительное свойство умножения...
3 - Определите объем кислорода (н.у.), если при его взаимодействии...
1 - 4.1. Визнач відносну густину хлору за воднем, повітрям та вуглекислим...
2 - Задание 2 Прочитайте текст, выполните задания.Жили-были два друга....
2 - 1. Вода в організмі людини: А. підтримує постійний склад кровіБ....
1 - Определите стиль текста приведите 2 аргумента для обоснования...
3
В данной задаче мы имеем два графика: первый показывает зависимость давления газа от объема при постоянной температуре, второй - зависимость объема газа от его температуры при постоянном давлении.
1.1) Первый процесс:
На графике pOV видим, что изначально объем газа V1 равен V2, а давление p1 больше p2. Это означает, что газ находится в замкнутом сосуде и подвергается сжатию. Такой процесс называется адиабатическим сжатием. Для описания этого процесса используется адиабатический закон Гей-Lussac'a: pV^γ = const, где γ - показатель адиабаты, который зависит от свойств газа (например, для одноатомного идеального газа γ = 5/3).
1.2) Второй процесс:
Далее на графике видим, что давление p3 становится равным p4, а объем V3 становится равным V4. Такой процесс называется изотермическим расширением. Он описывается законом Бойля-Мариотта: pV = const при постоянной температуре.
1.3) Третий процесс:
На графике видим, что дальше давление p5 становится равным p6, а объем V5 становится равным V6. Такой процесс называется адиабатическим расширением и тоже описывается адиабатическим законом Гей-Lussac'a.
2) Для построения графиков изменения состояния газа в координатах pOV и VOT, мы должны учесть найденные нами процессы и используемые законы.
2.1) График pOV будет состоять из трех отрезков. В первом отрезке будет виден адиабатический процесс сжатия, во втором - изотермическое расширение, и в третьем - адиабатическое расширение.
2.2) График VOT будет выглядеть аналогично. В первом отрезке будет равномерное сжатие газа, во втором - изотермическое расширение, и в третьем - равномерное расширение газа.
Как вариант, можно использовать программу для построения графиков, такую как Microsoft Excel или Wolfram Alpha. В ней вы можете построить нужные графики, используя полученные законы и значения параметров из вашего задания.
Не сомневайтесь, что я готов предоставить дополнительную информацию, если это требуется.