Одноатомный газ заключён в вместимостью 50л.при изохорном нагревании его давление возросло на 0,6 мпа.определить количество теплоты, сообщенное газу, и изменение его внутренней энергии.
Другие вопросы по теме Физика
Популярные вопросы
- Симметричную монету бросили пять раз. найдите вероятность события...
3 - Сочинение на тему: violent sport...
3 - Сочинение-рассуждение по произведению анна каренина на тему: возможно,...
3 - Напишите: отношение к экватору австралии, африки отношение к начальным...
1 - Cоставить диалог в формате огэ на тему english learning, отвечая...
2 - Укажите процессы окисления а)s+ s-2 б)s- s+4 в)mn+ mn+7 г) 2o-2...
1 - Общая площадь 79кв.м 1/2доля-собственник,1/8 другой,3/8третий...
2 - Изобразить криволинейную трапецию ограниченную осью ox прямыми...
2 - Угол а равнобедренной трапеции abcd равен 75 градусов. из точки...
3 - Insert to where necessary. help pleas...
3
При изохорическом процессе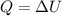 , где Q - количество теплоты (Дж), ΔU - изменение внутриней энергии (Дж). Получаем что, количество теплоы равно изменению внутриней энергии.
, где Q - количество теплоты (Дж), ΔU - изменение внутриней энергии (Дж). Получаем что, количество теплоы равно изменению внутриней энергии.
Внутренюю энергию одноатомного газа определяем по формуле: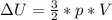 , где V - объём (м³), р - давление (Па). В системе СИ: 50 л = 0,05 м³;
, где V - объём (м³), р - давление (Па). В системе СИ: 50 л = 0,05 м³;
0,6 МПа = 6*10⁵ Па. Подставляем численные значения и вычисляем:
Процесс изохорный => V=const. (Обьем не изменен => работа не совершается)
Q=дельтаU+A' (A' у нас равен 0)
Q=дельтаU
для нахождения теплоты переданной газу, достаточно найти изменение внутренней энегрии газа (это дельта U)
дельтаU=(3/2)*(m/M)*R*(T2-T1)
( это ключевая формула, но мы в ней ничего не знаем, надо выразить все через те велечины что даны)
запишем уровнение Менделеева-Клапейрона для двух состояний, до нагревания и после
p1*V=(m/M)*R*T1
p2*V=(m/M)*R*T2 (V у нас не меняется,p1-давление газа до нагревания, T1-температура до нагревания)
вычетаем из второго уравниения первое получаем
(p2-p1)*V=(m/M)*R*(T2-T1)
изменение p2-p1 мы знаем 0,6 МПа.
мы можем подставить это в
дельтаU=(3/2)*(m/M)*R*(T2-T1)
получаем дельтаU=(3/2)*(p2-p1)*V
дельта U=(3/2)*0,6*(10^(-3))*50*10^(-3)=4.5*10^(-5) дж