Одноатомному газу изобарически передали 240 кДж тепла. На сколько
изменилась внутренняя энеригия (кДж) газа.
Другие вопросы по теме Физика
Популярные вопросы
- Найдите число ,которое составляет 4% от 4,5 найдите число ,которое составляет...
3 - Решите уравнение ( -31/21х+5/7)-1/3=-2,4/7...
1 - 5предложений из с прерывистой прямой речью....
2 - Вот вопросы: 1. что влияет на объем и структуру потребительских расходов?...
2 - А)8*(1,4x+13,6y)+13*(0,8x-0,6y)при x=1: y=1...
2 - 10.what do you do when you are buying a new dress? 11. where do you buy...
3 - Вычислить объем кислорода, при нормальных условиях, который потребуется...
2 - 3cos2x=4sinxcosx-sin2x решить, уравнение смешанного типа...
1 - Суммы всех коэффициентов в полном и сокращенном ионных уравнениях реакции...
2 - Обьяснить пословицу старого воробья и на мекине не проведешь...
1
144 кДж
Объяснение:
Первое начало термодинамики
Для изобарного процесса:
-работа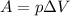
- изменение внутренней энергии (для одноатомного)
Имеем
Откуда
Откуда изменение внутренне энергии
Объяснение:
Количество теплоты при изобарическом процессе:
Q = ν·R·ΔT·(i/2+1)
Изменение внутренней энергии при изобарическом процессе:
ΔU = (i/2)·ν·R·ΔT
Работа при изобарическом процессе:
А = ν·R·ΔT
Как мы видим:
ΔU / Q = (i/2) / (i/2 + 1)
Для одноатомного газа i = 3.
Имеем:
ΔU / Q = (i/2) / (i/2 + 1) = 1,5 / 2,5 = 0,6
ΔU = 240·0,6 = 144 кДж