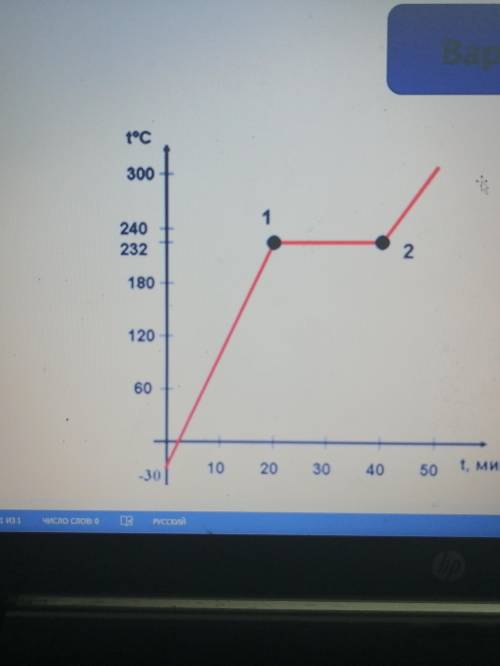
Какие процессы мы наблюдаем на графике Определите, какое это вещество
По графику определите количество теплоты, которое необходимо затратить, чтобы перевести данное вещество в другое агрегатное состояние массой 200г, если первоначальная температура (-20)°с
Другие вопросы по теме Физика
Популярные вопросы
- Втреугольнике abc угол а равен 70, внешний угол при вершине в...
3 - Составить слова существительные с основой на и...
1 - Іть будь у кіоск завезли однакову кількість ящиків з помідорами....
3 - Спеши предложения. 1мама испекла пирог с черникой. 2ваня вышел...
2 - Записать выражение и вычислите его значение: произведение чисел...
3 - Abc ! 1.5. дан одномерный массив а(n). отсортировать массив по...
3 - √4x^2+5x-2=2 найти произведение корней уравнения....
2 - 6. прочитай внимательно слова. какие из них «заблудились»? распредели...
1 - Впервом амбара было в 4 раза больше сна , чем втором. после того,...
3 - Вшколе 70% учеников любит играть футбол,50% любят играть в баскетбол...
1
1. Вначале видим, что температура вещества начинает возрастать в районе -20°C и достигает 0°C. Этот процесс называется нагреванием и происходит при постоянной температуре. В данном случае вещество находится в твердом агрегатном состоянии, так как мы меняем его температуру, не изменяя его агрегатное состояние.
2. После достижения температуры 0°C происходит плавление. Это процесс, при котором твердое вещество становится жидкостью при постоянной температуре. Мы видим на графике, что во время плавления температура не изменяется, а затрачивается теплота. В данном случае вещество находится в агрегатном состоянии твердо-жидкость.
3. После плавления следует нагревание жидкости. На графике видно, что температура жидкости увеличивается до 100°C. В это время мы не наблюдаем изменений в агрегатном состоянии, поэтому жидкость остается в том же состоянии.
4. Последний процесс на графике - это кипение. При достижении температуры кипения воды (100°C) происходит переход из жидкого состояния в газообразное состояние. В этом случае на графике также видно, что температура не изменяется, а затрачивается теплота. Вещество находится в агрегатном состоянии жидкость-газ.
Теперь перейдем к определению количества теплоты, которое необходимо затратить, чтобы перевести данное вещество массой 200 г из одного агрегатного состояния в другое. Для этого мы можем использовать формулу:
Q = m * C * ΔT
где Q - количество теплоты, m - масса вещества, C - удельная теплоемкость вещества, ΔT - изменение температуры.
Для твердого вещества (nagrevanie) удельная теплоемкость равна C1 = 2.1 Дж/(г*°C),
для плавления (plavlenie) C2 = 333 Дж/г,
для жидкости (zhidkost) C3 = 4.2 Дж/(г*°C),
и для кипения (kipenie) C4 = 2.26 Дж/г.
Исходя из графика, имеем:
-20°C -> 0°C (nagrevanie) ΔT1 = 0 - (-20) = 20°C
0°C (plavlenie) ΔT2 = 0
0°C -> 100°C (zhidkost) ΔT3 = 100 - 0 = 100°C
100°C (kipenie) ΔT4 = 0
Теперь можем посчитать количество теплоты для каждого процесса:
Q1 = m * C1 * ΔT1
Q2 = m * C2 * ΔT2
Q3 = m * C3 * ΔT3
Q4 = m * C4 * ΔT4
Суммируем все полученные значения:
Q = Q1 + Q2 + Q3 + Q4
Применяем формулы:
Q = 200 * 2.1 * 20 + 200 * 333 * 0 + 200 * 4.2 * 100 + 200 * 2.26 * 0
Выполняем вычисления:
Q = 8400 + 0 + 84000 + 0
Q = 92400 Дж
Таким образом, чтобы перевести данное вещество массой 200 г изначально при температуре -20°C в другое агрегатное состояние, необходимо затратить 92400 Дж теплоты.